
|
学习小专题 |
 盖斯定律及反应热的简单计算专练
日期:2021-06-24 16:10:16
点击:353
好评:0
盖斯定律及反应热的简单计算专练
日期:2021-06-24 16:10:16
点击:353
好评:0
盖斯定律及反应热的简单计算专练。...
 盖斯定律的有效应用
日期:2020-12-12 11:17:59
点击:12479
好评:0
盖斯定律的有效应用
日期:2020-12-12 11:17:59
点击:12479
好评:0
盖斯定律:实际上就是焓变的 加减 (概念:化学反应分成 二步 或 分几步 完成,总反应的 D H 等于各分步反应的 代数和 ) 如:试利用298K时下列反应焓变的实验数据,计算在此温度下 C(s)+O 2 (g)=CO(g)的反应焓变? 反应3 C(s)+ O 2 (g)=CO 2 (g) △H 1 =-393.5 KJmol ...
 乐乐课堂:盖斯定律应用
日期:2020-01-27 16:22:37
点击:579
好评:0
乐乐课堂:盖斯定律应用
日期:2020-01-27 16:22:37
点击:579
好评:0
第1集:盖斯定律内容与证明 第2集:盖斯定律的应用1 第3集:盖斯定律的应用2 第4集:盖斯定律的应用3...
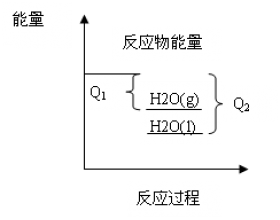 例谈反应热大小比较的两种方法
日期:2018-10-08 20:56:48
点击:4568
好评:0
例谈反应热大小比较的两种方法
日期:2018-10-08 20:56:48
点击:4568
好评:0
反应热大小比较是化学反应和能量变化这部分的常考题型,好多同学对这类题感觉无从下手,在这里介绍两种方法,希望能对读者起到帮助。 在这一章中经常会遇到这样的题: 在同温同压下,下列各组热化学方程式 Q 2 > Q 1 的是( ) A.2H 2 (g)+O 2 (g)=2H 2 O(g) ⊿H=- Q 1...
 盖斯定律计算反应热的注意事项
日期:2018-10-08 20:56:11
点击:3584
好评:0
盖斯定律计算反应热的注意事项
日期:2018-10-08 20:56:11
点击:3584
好评:0
化学反应的反应热只与始态和终态有关,而与反应途径无关,利用盖斯定律可以间接计算某些反应的反应热。 1.明确所求反应的始态和终态,各物质系数,及反应是吸热还是放热反应。 2.盖斯定律与反应途径无关,不同途径对应的最终结果是一样的。 3.各反应式相加时,有的反应...
 微课视频: 盖斯定律型反应热的计算
日期:2018-10-08 20:00:31
点击:413
好评:0
微课视频: 盖斯定律型反应热的计算
日期:2018-10-08 20:00:31
点击:413
好评:0
微课视频: 盖斯定律型反应热的计算。...
 热化学方程式正误判断及盖斯定律应用
日期:2016-01-31 20:18:04
点击:1929
好评:0
热化学方程式正误判断及盖斯定律应用
日期:2016-01-31 20:18:04
点击:1929
好评:0
一、热化学方程式的检查方法-------“四查” 查状态 查正负号 查单位 查匹配 三、盖斯定律的应用----关键是目标方程式的“四则运算式”的导出。 同类物质(同为反应物或同为生成物),反应热相加;不同类物质(一个为反应物与一个为生成物,反应热相减;反应方向倒转后...
 反应热与盖斯定律基础与专题
日期:2014-05-05 16:54:15
点击:356
好评:0
反应热与盖斯定律基础与专题
日期:2014-05-05 16:54:15
点击:356
好评:0
反应热与盖斯定律基础与专题...
 公开课短片-盖斯定律与反应焓变
日期:2013-05-03 11:12:16
点击:447
好评:0
公开课短片-盖斯定律与反应焓变
日期:2013-05-03 11:12:16
点击:447
好评:0
网易公开课视频-盖斯定律与反应焓变。来源于可汗学院,虽说是大学的基础化学内容,可做为高中阶段复习或扩展内容,很通俗易懂。...
 课件学习:盖斯定律
日期:2012-11-27 20:20:36
点击:399
好评:2
课件学习:盖斯定律
日期:2012-11-27 20:20:36
点击:399
好评:2
...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。