
|
学习小专题 |
 歧化反应与归中反应的几点质疑
日期:2016-11-09 09:26:40
点击:11611
好评:0
歧化反应与归中反应的几点质疑
日期:2016-11-09 09:26:40
点击:11611
好评:0
几个常见的歧化反应与归中反应。 歧化反应:同一物质中同一价态的同一元素发生的氧化还原反应。 Cl 2 +2OH - ==Cl - +ClO - +H 2 O,3Cl 2 +6OH - 5Cl - +Cl O 3 - +3H 2 O, 3S+6OH - S 2- +S O 3 2 - +3H 2 O,2Na 2 O 2 +2H 2 O==4NaOH+O 2 ↑, 2NO...
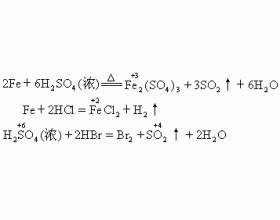 氧化产物和还原产物的判断
日期:2016-03-09 18:31:22
点击:14143
好评:0
氧化产物和还原产物的判断
日期:2016-03-09 18:31:22
点击:14143
好评:0
判断氧化产物和还原产物时,应抓住变价元素化合价的特征。当还原剂或氧化剂中所含变价元素的升降只存在一种可能时,它们的产物易于判断: ①非金属单质作氧化剂时,化合价变为负价(一般只有一个)。如,卤素由0价变为-1价,氧族元素由0价变为-2价,氮、磷由0价变为-3价...
 重要的氧化还原反应总结
日期:2016-01-17 21:08:49
点击:26313
好评:0
重要的氧化还原反应总结
日期:2016-01-17 21:08:49
点击:26313
好评:0
高中阶段所学的氧化还原反应可分为单质参与的反应和具有氧化性或还原性的重要化合物参与的反应两大类,下面我们简要回顾一下这两大类反应。 ⑴氧化性单质的反应 主要为O 2 、O 3 、卤素单质、S、N 2 、P等非金属单质参与的反应,以化合反应为主,其中应注意下面几个问题...
 氧化还原反应方程式书写专题训练
日期:2016-01-07 18:14:03
点击:6485
好评:0
氧化还原反应方程式书写专题训练
日期:2016-01-07 18:14:03
点击:6485
好评:0
向K 2 MnO 4 溶液中通入CO 2 ,可制得KMnO 4 ,同时产生黑色沉淀。 将Cl 2 通过二氧化钛和碳粉的混合物,可制得四氯化钛和一种有毒气体 NH 3 与NaClO反应可制N 2 H 4 ; 肼—空气燃料电池是一种碱性电池,电解质为KOH,则电池负极反应式 向CuCl 2 溶液中通入一定量的SO ...
 浅谈氧化还原反应产物的一般判断规则文档
日期:2015-08-05 14:42:50
点击:414
好评:0
浅谈氧化还原反应产物的一般判断规则文档
日期:2015-08-05 14:42:50
点击:414
好评:0
浅谈氧化还原反应产物的一般判断规则...
 陌生氧化还原反应方程式的书写专练
日期:2015-06-16 12:24:11
点击:613
好评:0
陌生氧化还原反应方程式的书写专练
日期:2015-06-16 12:24:11
点击:613
好评:0
陌生氧化还原反应方程式的书写专练...
 “四步法”书写陌生氧化还原反应方程式
日期:2014-05-07 15:12:34
点击:3445
好评:0
“四步法”书写陌生氧化还原反应方程式
日期:2014-05-07 15:12:34
点击:3445
好评:0
一、陌生氧化还原反应方程式的书写方法 1.“四步法”书写陌生氧化还原反应方程式 第一步:根据元素化合价的升降判断氧化剂、还原剂、氧化产物、还原产物。 第二步:按“氧化剂+还原剂=还原产物+氧化产物”写出方程式,根据得失电子守恒配平上述四种物质。注意:不属于“...
 中学阶段最重要的30类127个分子间氧化还原反应归纳
日期:2014-01-16 17:47:42
点击:526
好评:0
中学阶段最重要的30类127个分子间氧化还原反应归纳
日期:2014-01-16 17:47:42
点击:526
好评:0
中学阶段最重要的30类127个分子间氧化还原反应归纳...
 中学常见的氧化还原反应文档
日期:2014-01-13 16:04:34
点击:338
好评:0
中学常见的氧化还原反应文档
日期:2014-01-13 16:04:34
点击:338
好评:0
·中学常见的氧化还原反应...
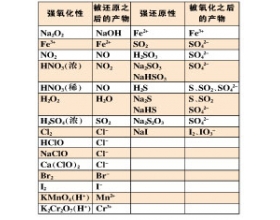 复杂氧化还原反应离子方程式
日期:2012-03-07 11:49:44
点击:22704
好评:0
复杂氧化还原反应离子方程式
日期:2012-03-07 11:49:44
点击:22704
好评:0
高中化学涉及的反应是以氧化还原反应为主题,又经常以离子方程式的形式来体现,在高考题中经常涉及的一些复杂氧化还原反应离子方程式的书写,对于高三学生来讲往往是一道不可逾越的墙,究竟有没有一种可行有效的方法解决这个问题呢?笔者通过对众多氧化还原反应的离子方...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。