
|
学习小专题 |
 铜、银在盐酸里能否形成原电池?
日期:2023-10-30 08:26:06
点击:15384
好评:0
铜、银在盐酸里能否形成原电池?
日期:2023-10-30 08:26:06
点击:15384
好评:0
锌跟盐酸反应,铜不跟盐酸反应.当把锌片、铜片插入盐酸并用导线连接起来,就形成了原电池,这是众所周知的.那么,铜和银都不跟盐酸反应,铜和银在盐酸里能不能形成原电池呢? [实验一]:用导线把铜片、电流计(mA)、银片依次串联起来.再把铜片、银片插入盐酸溶液中...
 学习课件:组成化学电池的条件
日期:2022-05-23 08:49:33
点击:308
好评:0
学习课件:组成化学电池的条件
日期:2022-05-23 08:49:33
点击:308
好评:0
...
 实验模拟:原电池实验探究
日期:2019-05-03 20:38:09
点击:602
好评:0
实验模拟:原电池实验探究
日期:2019-05-03 20:38:09
点击:602
好评:0
...
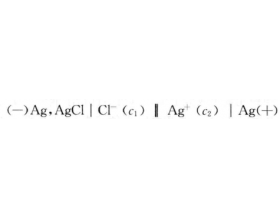 原电池构成的条件是什么?
日期:2018-08-05 16:38:58
点击:9235
好评:0
原电池构成的条件是什么?
日期:2018-08-05 16:38:58
点击:9235
好评:0
在中学化学教学中,“原电池原理及其应用”是高中化学课程中电化学知识部分的重要内容。在中学化学的教学中,多数化学教师习惯于帮助学生总 结归纳原电池构成的条件,绝大多数教师将原电池构成的条件总结成: (1)存在能自发进行的氧化还原反应; (2)两种活动性不同的金属材...
 如何理解原电池自发氧化还原反应?
日期:2017-09-29 21:25:34
点击:9792
好评:1
如何理解原电池自发氧化还原反应?
日期:2017-09-29 21:25:34
点击:9792
好评:1
原电池是把化学能转化为电能的装置。原电池中发生的反应是自发的氧化还原反应,这类反应必须满足反应物的总能量大于生成物的总能量,即放热反应。当然,这类氧化还原反应也满足自由能变ΔG 0或电池电动势大于零。...
 课件学习:原电池条件练习
日期:2017-04-26 09:43:35
点击:347
好评:0
课件学习:原电池条件练习
日期:2017-04-26 09:43:35
点击:347
好评:0
...
 原电池的构成条件
日期:2017-04-25 17:42:14
点击:4376
好评:0
原电池的构成条件
日期:2017-04-25 17:42:14
点击:4376
好评:0
(1)两 个导体分别作为正、负极。若电池为单液电池,两电极的 化学 性质须不相同;若电池为双液电池,则两电极可相同。 (2) 连通的电解质溶液构成两极间的内电路。两个电极插入同一电解质溶液,或分别插入两种不同的电解质溶液,再用盐桥连通。 构成原电池是否必须一...
 对原电池形成条件的思考
日期:2017-04-25 17:25:15
点击:974
好评:0
对原电池形成条件的思考
日期:2017-04-25 17:25:15
点击:974
好评:0
在选修与必修的衔接方面,必修2中介绍了原电池的装置和 原理,归纳了形成原电池的条件。选修4在此基础上,介绍较复杂 的带盐桥的原电池,进一步认识原电池的形成和反应原理,关注原 电池的使用价值。关于原电池形成条件的教学,我有以下思考供各 位同仁参考,不对之处敬...
 氯气、氢氧化钠溶液能形成原电池吗
日期:2015-05-27 20:53:33
点击:2260
好评:0
氯气、氢氧化钠溶液能形成原电池吗
日期:2015-05-27 20:53:33
点击:2260
好评:0
◇形成原电池的前提有四个 条件 1 :在体系中存在一个自发的放热的氧化还原反应。 条件 2 :存在电解质溶液或者熔融的电解质 条件 3 :组成一个闭合回路 条件 4 :两个电极(大部分情况这两个电极的材料应该是不相同的) ◇关于氢气和氧气燃料电池 1 、氢气和氧气反应是...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。