
|
学习小专题 |
 原电池图形题考点精评
日期:2022-05-09 08:20:03
点击:9791
好评:0
原电池图形题考点精评
日期:2022-05-09 08:20:03
点击:9791
好评:0
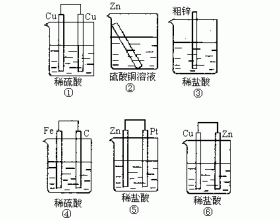
原电池图形题是考察学生基本知识、实验的观察及分析能力、实际生活知识三者结合在一起的综合能力题。最初学生掌握起来难度较大。下面以8个考点为主线进行分析。 一、判断是否形成原电池 牢记形成原电池的三个条件:①两个活动性不同的金属或金属和非金属(如石墨)做电...
 电极材料一定要参与反应吗?
日期:2021-12-21 14:05:55
点击:19364
好评:1
电极材料一定要参与反应吗?
日期:2021-12-21 14:05:55
点击:19364
好评:1
原电池是把化学能转化为电能的装置,在原电池的两极发生氧化还原反应因电子转移而产生电流。参加氧化还原反应的可以是电极材料本身,也可以是电极周围的物质,据此我们根据电极材料是否参加氧化还原反应把中学化学常见原电池分为三大类。 一. 仅有一电极材料参与反应...
 几种“反常”的原电池
日期:2021-12-21 14:00:16
点击:3587
好评:2
几种“反常”的原电池
日期:2021-12-21 14:00:16
点击:3587
好评:2
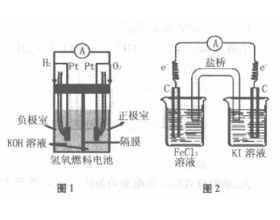
原电池是将化学能转变成电能的装置,构成 原电池的一般条件是: 1.两个活泼性不同的电极; 2.电解质溶液; 3.形成闭合回路; 4.能自发发生氧化还原反应。 通常是活泼的金属作负极,金属本身被氧化; 不活泼的金属或非金属作正极,溶液中的阳离子 被还原。 以上“一般”...
 新课程实验演示:原电池实验
日期:2021-10-19 17:12:45
点击:223
好评:0
新课程实验演示:原电池实验
日期:2021-10-19 17:12:45
点击:223
好评:0
...
 动画模拟:原电池原理微观模拟
日期:2021-01-22 08:59:03
点击:735
好评:0
动画模拟:原电池原理微观模拟
日期:2021-01-22 08:59:03
点击:735
好评:0
...
 乐乐课堂:原电池工作原理及应用
日期:2020-01-27 11:42:18
点击:778
好评:1
乐乐课堂:原电池工作原理及应用
日期:2020-01-27 11:42:18
点击:778
好评:1
第一集:原电池的工作原理 第二集:双液电池工作原理 第三集:原电池原理的应用...
 动画模拟:原电池工作原理
日期:2017-04-26 09:46:39
点击:2032
好评:4
动画模拟:原电池工作原理
日期:2017-04-26 09:46:39
点击:2032
好评:4
...
 原电池原理的自我理解
日期:2017-04-25 19:00:42
点击:7242
好评:0
原电池原理的自我理解
日期:2017-04-25 19:00:42
点击:7242
好评:0
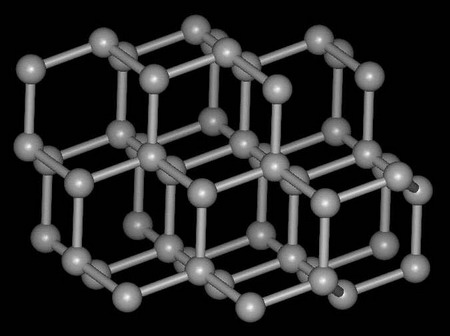
金属是由金属的阳离子和自由电子组合而成,自由电子可以在整块金属内部自由的移动,而金属阳离子的位置相对固定。活泼性不同的金属,其阳离子与自由电子间的作用力不同。但任何金属放置在水溶液中时,其表面均会受到水分子的撞击。势必会将一些阳离子撞击下来,使得金属...
 在原电池的内电路中,为什么不发生电子的直接交换?
日期:2017-04-17 09:32:31
点击:1725
好评:0
在原电池的内电路中,为什么不发生电子的直接交换?
日期:2017-04-17 09:32:31
点击:1725
好评:0
以铜-锌原电池为例。当锌与酸反应时锌失去电子,电子留在锌板上,锌离子进入溶液中,并在锌板周围形成锌离子“墙”,若氢离子要到锌板上获得电子时,必然要通过这道“墙”,由于锌离子对氢离子是互相排斥的,就使氢离子难以越过这道屏障,阻碍了氢离子得电子。但当用导线将...
 动画模拟:原电池微观模拟
日期:2012-11-27 20:28:58
点击:781
好评:0
动画模拟:原电池微观模拟
日期:2012-11-27 20:28:58
点击:781
好评:0
...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。