
|
学习小专题 |
 氯溴碘溶液颜色为啥越来越深
日期:2022-11-23 10:59:14
点击:597
好评:0
氯溴碘溶液颜色为啥越来越深
日期:2022-11-23 10:59:14
点击:597
好评:0
溴分子或碘分子属于非极性分子(所谓非极性分子就是对称性很很很好的分子)。CCl 4 就是一种对称性很很很好的分子,它是非极性的。相对而言,水的对称性要差一些,其是极性分子。 溴单质、碘单质如果溶解在非极性溶剂中,其颜色与单质颜色接近,就好比是被其稀释而已。如,溴...
 卤族元素及其化合物口诀
日期:2022-08-06 16:13:57
点击:15540
好评:0
卤族元素及其化合物口诀
日期:2022-08-06 16:13:57
点击:15540
好评:0
氯气有毒刺激性, 闻氯用手轻扇动。 热铜热铁遇氯气, 烟色相似皆为棕。 氢在氯中苍白焰, 磷在氯中烟雾漫。 甲烷氢气氯相混, 强光照射太危险。 氯水消毒又漂白, 作用原理次氯酸。 消石灰氯漂白粉, 用时常通二氧碳, 二氧化锰盐酸逢, 隔网热瓶氯气生。 盐水硫酸除杂...
 有关“氯的化合物”计算型选择题解法例析
日期:2022-08-05 17:27:54
点击:23013
好评:0
有关“氯的化合物”计算型选择题解法例析
日期:2022-08-05 17:27:54
点击:23013
好评:0
《卤素》计算型选择题解法例析 《卤素》是中学化学中最典型的一族非金属元素 ,学生在学习中对计算量大的选择题不会运用正确的方法,不去认真分析与计算而胡乱猜测。导致比较害怕这类试题,失去进一步学好化学的信心。其实这类选择题并不难,主要看能否运用巧妙的方法解答...
 元素发现史:卤素的发现及其单质的制取
日期:2022-08-01 15:01:55
点击:2091
好评:0
元素发现史:卤素的发现及其单质的制取
日期:2022-08-01 15:01:55
点击:2091
好评:0
一.发现元素就是发现其单质 除了那些人工放射性元素,历史上的“发现元素”是以什么为标志的?原始人类就知道吃盐了,是不是说人类从远古时代就已经发现了氯元素和钠元素呢?当然不是。 发现元素的标志其实是发现或制取了该元素的单质。氯元素是1774年发现的,就是在那...
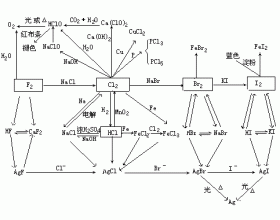 学法指导:卤素知识体系
日期:2020-03-05 11:55:21
点击:12682
好评:0
学法指导:卤素知识体系
日期:2020-03-05 11:55:21
点击:12682
好评:0
一、知识体系 上面知识体系能帮助读者掌握代表物 Cl 2 的制法、性质及其化合物 HCl 的制法、盐酸的性质、次氯酸的性质,并能掌握 F 2 、 Br 2 、 I 2 及其化合物的重要性质、制法和 X- 的鉴别。 二、重点、难点知识 在卤素中,氯最重要,性质最典型,是学习的重点。难...
 氯、溴、碘的正价为什么都是奇数价?
日期:2017-04-17 15:11:08
点击:2346
好评:0
氯、溴、碘的正价为什么都是奇数价?
日期:2017-04-17 15:11:08
点击:2346
好评:0
卤素原子只有一个未成对电子,当其与电负性更强的原子结合时,失去一个未成对的电子而呈+1价。当p轨道上的1对成对电子激发到空的d轨道后即进行sp 3 d杂化,这样就有三个未成对电子,成键时显+3价,以此类推,分别进行sp 3 d 2 和sp 3 d 3 杂化,成键时卤素的化合价为+5、...
 化学元素趣闻―卤族元素
日期:2014-04-24 09:32:21
点击:25689
好评:0
化学元素趣闻―卤族元素
日期:2014-04-24 09:32:21
点击:25689
好评:0
在所有的元素中,要算氟最活泼了 。 氟是淡黄色的气体,有特殊难闻的臭味,剧毒。在- 188℃以下,凝成黄色的液体。在-223℃变成黄色结晶体。在常温下,氟几乎能和所有的元素化合:大多数金属都会被氟腐蚀,碱金属在氟气中会燃烧,甚至连黄金在受热后,也能在氟气中燃烧...
 情景素材-氟气与金属铯化合反应
日期:2013-10-18 16:02:31
点击:465
好评:0
情景素材-氟气与金属铯化合反应
日期:2013-10-18 16:02:31
点击:465
好评:0
最疯狂而最简单的化合反应,一个在著名的英国贵族研究型学府---莱切斯特大学里的化学实验室里进行的实验。...
 氟与碘的特殊性
日期:2013-04-16 10:58:20
点击:12418
好评:0
氟与碘的特殊性
日期:2013-04-16 10:58:20
点击:12418
好评:0
一、氟的特殊性 1.氟是所有元素中非金属性最强、电负性最大的元素,因此F与Cl、Br、I不同,它没有正化合价,它的含氧酸只有HFO,且HFO中F为-1价; 2.卤素单质在水中的溶解度不大,其中F 2 不溶于水,与水剧烈反应生成HF和O 2 ,因此将F 2 通入其他卤化物的水溶液中,F 2...
 卤素单质在不同溶剂中所形成溶液(从稀到浓)的颜色变化
日期:2013-02-27 10:38:55
点击:5352
好评:0
卤素单质在不同溶剂中所形成溶液(从稀到浓)的颜色变化
日期:2013-02-27 10:38:55
点击:5352
好评:0
溴和碘在不同溶剂中所形成溶液(从稀到浓)的颜色变化 水 苯(或汽油) 四氯化碳 溴 黄→棕 橙→橙红 橙→橙红 碘 深黄→褐 淡紫→紫红 紫→深紫 注:碘溶于酒精后,溶液呈褐色。 需要说明的是,溴水、碘水由于浓度不同,其溶液的颜色可能相同也可能不同。但在有机溶剂中肯定不...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。