
|
学习小专题 |

|
学习小专题 |
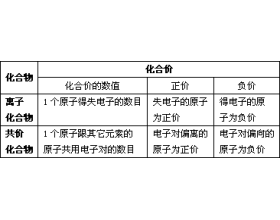 [注解与辨疑y] 化合价知识解析 作者:化学自习室 来源:未知 日期:2023-09-14 16:17:42 点击:499 所属专题:化合价
[注解与辨疑y] 化合价知识解析 作者:化学自习室 来源:未知 日期:2023-09-14 16:17:42 点击:499 所属专题:化合价
化合价 化合价是一种元素的一个原子与其他元素的原子化合【即构成化合物】时表现出来的性质。一般的,化合价的价数等于每个该原子在化合时得失电子的数量,即该元素能达到稳定结构时得失电子的数量,这往往决定于该元素的电子排布,主要是最外层电子排布,当然还可能涉...
 [注解与辨疑y] 常见的氧化剂、还原剂 作者:化学自习室 来源:未知 日期:2022-11-21 17:41:51 点击:528 所属专题:氧化剂 还原剂
[注解与辨疑y] 常见的氧化剂、还原剂 作者:化学自习室 来源:未知 日期:2022-11-21 17:41:51 点击:528 所属专题:氧化剂 还原剂
氧化剂 还原剂 活泼非金属单质:X 2 、O 2 、S 活泼金属单质:Na、Mg、Al、Zn、Fe 某些非金属单质:C、H 2 、S 高价金属离子:Fe 3+ 、Sn 4+ 不活泼金属离子:Cu 2+ 、Ag + 其它:[Ag(NH 3 ) 2 ]+、新制Cu(OH) 2 低价金属离子:Fe 2+ 、Sn 2+ 非金属的阴离子及其化...
 [注解与辨疑y] 高中化学氧化性强弱顺序最全 作者:化学自习室 来源:未知 日期:2021-11-22 07:56:40 点击:48848 所属专题:氧化性
[注解与辨疑y] 高中化学氧化性强弱顺序最全 作者:化学自习室 来源:未知 日期:2021-11-22 07:56:40 点击:48848 所属专题:氧化性
非金属单质氧化性: 一般情况下元素非金属性强的对应的单质氧化性强。 例如:非金属性F>Cl>Br>I>S,则氧化性F 2 >Cl 2 >Br 2 >I 2 >S 1、同周期(横行,从左到右)元素非金属性递增,单质氧化性增强。 2、同主族(竖行,从上到下)元素非金属性递减,单质氧化性递减...
 [注解与辨疑y] 氧化还原反应规律释疑 作者:王笃年 来源:未知 日期:2021-11-09 09:39:41 点击:556 所属专题:氧化还原反应规律
[注解与辨疑y] 氧化还原反应规律释疑 作者:王笃年 来源:未知 日期:2021-11-09 09:39:41 点击:556 所属专题:氧化还原反应规律
氧化还原反应是一类重要的化学反应,其中蕴涵 着“对立统一”等哲学思想.氧化还原反应中有一些重 要的规律,有的比较容易理解,如“有氧化必有还原”、 “氧化剂得电子总数等于还原剂失电子总数等,而有 的规律如果不加深入思考则较难理解. 1、如何理解“在自发的氧化还原反...
 [注解与辨疑y] 氧化剂为什么要强调在酸性溶液中使用? 作者:化学自习室 来源:未知 日期:2021-08-18 15:27:09 点击:648 所属专题:氧化剂
[注解与辨疑y] 氧化剂为什么要强调在酸性溶液中使用? 作者:化学自习室 来源:未知 日期:2021-08-18 15:27:09 点击:648 所属专题:氧化剂
溶液的酸碱性对许多化学反应有很大的影响,在中学化学教学中经常会遇到这方面的例子: 实验室用MnO 2 与浓盆酸反应制备少量氯气: MnO 2 +4 H + + 2Cl - ==Mn 2 ++ 2H 2 O+Cl 2 检验乙烯通常用酸性KMnO 4 溶液。 用Cu(OH) 2 的强碱性溶液检验醛基。 在氧化还原反...
 [注解与辨疑y] 氧化还原反应终极总结 作者:化学自习室 来源:未知 日期:2021-06-15 16:16:12 点击:2547 所属专题:氧化还原反应
[注解与辨疑y] 氧化还原反应终极总结 作者:化学自习室 来源:未知 日期:2021-06-15 16:16:12 点击:2547 所属专题:氧化还原反应
一、氧化还原反应的基本概念 1. 氧化还原反应的本质 : 有电子转移 (得失) 氧化还原反应概念图 2. 氧化还原反应的特征 : 元素化合价的变化 应用: 在化学方程式中标出各物质组成元素的化合价,只要有一种元素的化合价发生了变化,即可说明该反应是氧化还原反应。 口...
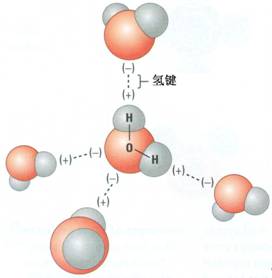 [注解与辨疑y] 氧化还原反应概念认识误区 作者:化学自习室 来源:未知 日期:2020-06-13 11:10:47 点击:546 所属专题:氧化还原反应概念
[注解与辨疑y] 氧化还原反应概念认识误区 作者:化学自习室 来源:未知 日期:2020-06-13 11:10:47 点击:546 所属专题:氧化还原反应概念
1.误认为有单质参与或生成的反应一定是氧化还原反应。如O 2 与O 3 的转化为非氧化还原反应。 2.误认为元素由化合态变为游离态一定被还原,其实不一定。如HCl→Cl 2 ,氯元素被氧化,CuO→Cu,铜元素被还原。 3.误认为氧化还原反应中有一种元素被氧化,则一定有另一种元素...
 [注解与辨疑y] 高锰酸钾性质解读 作者:张劲辉 来源:未知 日期:2019-01-08 15:50:44 点击:1519 所属专题:高锰酸钾
[注解与辨疑y] 高锰酸钾性质解读 作者:张劲辉 来源:未知 日期:2019-01-08 15:50:44 点击:1519 所属专题:高锰酸钾
高锰酸钾在不同条件下的颜色变化 高锰酸钾与亚硫酸钠反应: 高锰酸钾与碘化钾为反应:...
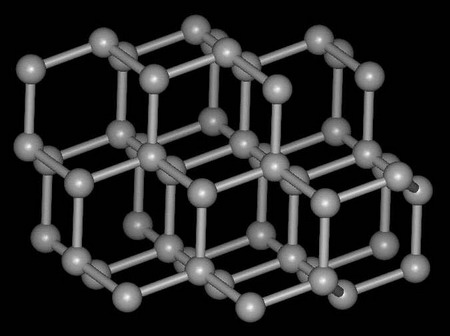 [注解与辨疑y] 我给氧化剂评“职称” 作者:骆传汉 来源:未知 日期:2018-10-14 21:05:21 点击:915 所属专题:氧化剂
[注解与辨疑y] 我给氧化剂评“职称” 作者:骆传汉 来源:未知 日期:2018-10-14 21:05:21 点击:915 所属专题:氧化剂
据物质在反应中的表现我们给常见的物质评“职称”: “特级”氧化剂 (ClO - 、S 2 O 8 2 - 、NaBiO 3 , PbO 2 ) + H + …… “高级”氧化剂 ( Cr 2 O 7 2 - 、Fe O 4 2 - 、Mn O 4 - 、N O 3 - ) +H + 、 F 2 、O 3 …… “一级”氧化剂 ClO 2 、Ni 2 O 3 、CO 2...
 [注解与辨疑y] 溶液酸碱性对氧化还原反应有影响吗? 作者:吴星 来源:未知 日期:2018-08-05 17:14:48 点击:13135 所属专题:氧化产物 还原产物
[注解与辨疑y] 溶液酸碱性对氧化还原反应有影响吗? 作者:吴星 来源:未知 日期:2018-08-05 17:14:48 点击:13135 所属专题:氧化产物 还原产物
溶液的酸碱性对许多化学反应有很大的影响,在中学化学教学中经常会遇到这方面的例子: 实验室用MnO 2 与浓盆酸反应制备少量氯气: MnO 2 +4 H + + 2Cl - ==Mn 2 ++ 2H 2 O+Cl 2 检验乙烯通常用酸性KMnO 4 溶液。 用Cu(OH) 2 的强碱性溶液检验醛基。 在氧化还原反...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。化合价 化合价是一种元素的一个原子与其他元素的原子化合【即构成化合物】时表现出来...
氧化剂 还原剂 活泼非金属单质:X 2 、O 2 、S 活泼金属单质:Na、Mg、Al、Zn、Fe 某...
常见阴离子还原性强弱顺序:S 2- SO 3 2- I - Fe 2+ Br - Cl - OH - 含氧酸根 F - 最常...
1. 得电子物质被还原是氧化剂。 2. 失e物质、被还原、发生了还原反应。 3. 氧化剂...
常见的强氧化剂简介 具有强烈氧化性的物质。在标准电位顺序中的位置越靠后,标准电位...
非金属单质氧化性: 一般情况下元素非金属性强的对应的单质氧化性强。 例如:非金属性...
氧化还原反应是一类重要的化学反应,其中蕴涵 着“对立统一”等哲学思想.氧化还原反应...
以下几类特殊的氧化还原反应在教与学中值得专题讨论: 一、部分氧化还原反应 在氧化还...