
|
ѧϰСר�� |

|
ѧϰСר�� |
 [ע�������h] ���Ⱥ����ȵľ������ ����:���˻� ��Դ:δ֪ ���ڣ�2015-12-11 19:46:43 �����1194 ����ר�⣺���ȷ�Ӧ ���ȷ�Ӧ
[ע�������h] ���Ⱥ����ȵľ������ ����:���˻� ��Դ:δ֪ ���ڣ�2015-12-11 19:46:43 �����1194 ����ר�⣺���ȷ�Ӧ ���ȷ�Ӧ
һ������£�����ķ�Ӧ�����ȵģ���ֽ⡢��⣨���룩��ˮ�⡢���ȣ���֮���ϵķ�Ӧ���ȣ��绯�ϡ���ϣ����ӽ�ϳ����塢������������ʣ��ȡ� ��Ϊ������ԭ��Ӧ�������Ի�ԭ��ǿ������֮�䷴Ӧ���������Ի�ԭ���������ʶ��Ƿ��ȵģ���֮�����ȵġ�...
 [ע�������h] ��ȼ���йص����⼯ ����:��Ϧ ��Դ:δ֪ ���ڣ�2015-12-11 19:47:54 �����574 ����ר�⣺ȼ��
[ע�������h] ��ȼ���йص����⼯ ����:��Ϧ ��Դ:δ֪ ���ڣ�2015-12-11 19:47:54 �����574 ����ר�⣺ȼ��
һ�����ȼ����ָ��ȼ��������������һ�ַ�����ȵľ��ҵ�������Ӧ�� ����ȼ�յ��������������ʾ��п�ȼ�ԣ���ȼ������������������Ӵ����¶ȴﵽ��ȼ����Ż�� ���� �ٽ�����ȼ�յķ����� ��1������������Ũ�ȣ� ��2�������ȼ���������ĽӴ���� �ġ� ��ȼ�ո���...
 [ע�������h] ��H����������������ȹ�ϵ������� ����:���� ��Դ:δ֪ ���ڣ�2016-01-31 20:12:17 �����17660 ����ר�⣺�ʱ�
[ע�������h] ��H����������������ȹ�ϵ������� ����:���� ��Դ:δ֪ ���ڣ�2016-01-31 20:12:17 �����17660 ����ר�⣺�ʱ�
ѧ�������Ȼ�ѧ�е����ȷ�Ӧ�ͷ��ȷ�Ӧ�������仯�������ʮ������������������ȷ�Ӧ �� H ���� 0 �������ȷ�Ӧ �� H С�� 0 �����ȷ�Ӧ�����ȷ�Ӧ�з�Ӧ�����������������С��ϵ������һ֪��⣬����Ū���ҡ�Ϊ����ѧ���������Ū����Щ���⣬���ڽ�ѧ������������...
 [ע�������h] �ʵ�����ʲô�� ����:��� ��Դ:δ֪ ���ڣ�2014-09-04 16:41:34 �����706 ����ר�⣺�ʱ�
[ע�������h] �ʵ�����ʲô�� ����:��� ��Դ:δ֪ ���ڣ�2014-09-04 16:41:34 �����706 ����ר�⣺�ʱ�
...
 [ע�������h] �Ȼ�ѧ����ʽ�����жϼ���˹����Ӧ�� ����:³Ⱥ ��Դ:δ֪ ���ڣ�2016-01-31 20:18:04 �����1704 ����ר�⣺�Ȼ�ѧ����ʽ ��˹����
[ע�������h] �Ȼ�ѧ����ʽ�����жϼ���˹����Ӧ�� ����:³Ⱥ ��Դ:δ֪ ���ڣ�2016-01-31 20:18:04 �����1704 ����ר�⣺�Ȼ�ѧ����ʽ ��˹����
һ���Ȼ�ѧ����ʽ�ļ�鷽��-------���IJ顱 ��״̬ �������� �鵥λ ��ƥ�� ������˹���ɵ�Ӧ��----�ؼ���Ŀ�귽��ʽ�ġ���������ʽ���ĵ����� ͬ�����ʣ�ͬΪ��Ӧ���ͬΪ���������Ӧ����ӣ���ͬ�����ʣ�һ��Ϊ��Ӧ����һ��Ϊ�������Ӧ���������Ӧ����ת��...
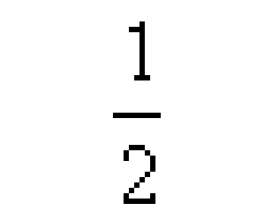 [ע�������h] �Ȼ�ѧ����ʽ���ص����� ����:������ ��Դ:δ֪ ���ڣ�2016-01-31 20:20:00 �����7084 ����ר�⣺�Ȼ�ѧ����ʽ
[ע�������h] �Ȼ�ѧ����ʽ���ص����� ����:������ ��Դ:δ֪ ���ڣ�2016-01-31 20:20:00 �����7084 ����ר�⣺�Ȼ�ѧ����ʽ
H 2 �� g �� +1�M2O 2 �� g �� =H 2 O �� l �� �� H �� 298K �� = �� 285.8KJ��mol �� 1 ���˷�Ӧ������ʾ�����ʵı仯������ʾ�˷�Ӧ���ʱ䣬�˷���ʽΪ�Ȼ�ѧ����ʽ�� 1 ���Ȼ�ѧ����ʽ������Ȼ�ѧ�У�����ѧ��Ӧ�����ʵı仯�ͷ�Ӧ���ʱ�ͬʱ��ʾ�����Ļ�ѧ����ʽ...
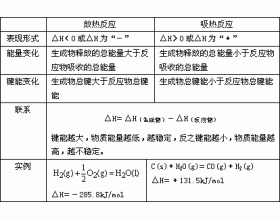 [ע�������h] ��ѧ��Ӧ���Ȼ����ȵ��ж� ����:��ѧ�� ��Դ:δ֪ ���ڣ�2016-01-31 20:26:07 �����9216 ����ר�⣺���ȷ�Ӧ ���ȷ�Ӧ
[ע�������h] ��ѧ��Ӧ���Ȼ����ȵ��ж� ����:��ѧ�� ��Դ:δ֪ ���ڣ�2016-01-31 20:26:07 �����9216 ����ר�⣺���ȷ�Ӧ ���ȷ�Ӧ
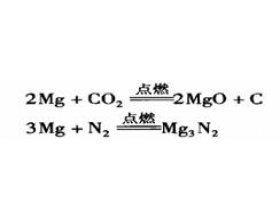
1�����ݾ��廯ѧ��Ӧʵ���ж� ��1�������ķ��ȷ�Ӧ�����п�ȼ���ȼ�ա����н�������ķ�Ӧ�������кͷ�Ӧ������������Ϸ�Ӧ�������ֽⷴӦ�������û���Ӧ�����ȷ�Ӧ��ijЩ���ֽⷴӦ�����ͷ�Ӧ�� ��2�����������ȷ�Ӧ��������Ļ��Ϸ�Ӧ��CO 2 ��C�ķ�Ӧ�����������...
 [ע�������h] ��ѧ��Ӧ�ķ�Ӧ������ܵĹ�ϵ ����:��� ��Դ:δ֪ ���ڣ�2018-10-08 20:57:22 �����22748 ����ר�⣺��Ӧ�ȼ��� ����
[ע�������h] ��ѧ��Ӧ�ķ�Ӧ������ܵĹ�ϵ ����:��� ��Դ:δ֪ ���ڣ�2018-10-08 20:57:22 �����22748 ����ר�⣺��Ӧ�ȼ��� ����
�½̲��й��ڷ�Ӧ�ȵĶ�����ɽ̲���ȣ���Ϊ��ѧ�����������ھɽ̲ĵ�Ӱ�죬���������½̲ĵĽ�ѧ�����У��������ڶ�IJο������ϣ��������Ÿ��ָ���ģ�������Ǵ���Ĺ۵㡣���磬��ȫ��Ӱ��ϴ��־���Ż�����°������ϰ�����ϣ���ѧ��Ӧ����ЧӦ H =������ļ�����...
 [ע�������h] ��ȷ��ʶ���ʵ�ȼ�� ����:�Ű� ��Դ:δ֪ ���ڣ�2016-01-31 20:41:04 �����8674 ����ר�⣺ȼ��
[ע�������h] ��ȷ��ʶ���ʵ�ȼ�� ����:�Ű� ��Դ:δ֪ ���ڣ�2016-01-31 20:41:04 �����8674 ����ר�⣺ȼ��
һ������ȼ��һ����Ҫ������? 1.ȼ��ͨ��ָ���ǿ�ȼ��������е�����������һ�ַ��ⷢ�ȵľ��ҵĻ�ѧ��ӦɨӦ�ý��������ʵ�ȼ����Ҫ����֧�֡�����ͨ����˵��ȼ�ն�ָ��ȼ���ڿ����е�ȼ�գ������͡��ƾ���ú��ʯ�������ʵ�ȼ�ա� 2.�ӹ����Ͻ���ȼ����һ�ַ��ⷢ�ȵ�...
 [ע�������h] ȼ���Ƚ�� ����:������ ��Դ:δ֪ ���ڣ�2016-01-31 20:44:01 �����6519 ����ר�⣺ȼ����
[ע�������h] ȼ���Ƚ�� ����:������ ��Դ:δ֪ ���ڣ�2016-01-31 20:44:01 �����6519 ����ר�⣺ȼ����
һ��ȼ���ȸ��� ��101KPa ʱ��1mol ������ȫȼ�������ȶ���������ʱ�����ų����������������ʵ�ȼ���ȡ�ȼ�����Ƿ�Ӧ�ȵ�һ����ʽ��ͨ����ʵ��ⶨ����λ��KJ��mol -1 �� KJ/ mol ����ȼ���ȵ�Ҫ�� 1���涨����101 kPaѹǿ�²���������̲��ṩ��ȼ�������ݶ�����101kPa...
 ��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ�
��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ� ��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء�
��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء�1.����ʲô����ʲô�����йأ����ʵľ�����ֵ�Ƿ�ɲ⣿ ��(����H)��һ������˵�����...
...
��һ�Σ����ӷ�Ӧ������������Ҫ�г��������塢ˮ���ɣ� �ڶ��Σ����ӷ�Ӧ������...
��Ӧ�� ����ѧ��Ӧ��һ���¶��½���ʱ����Ӧ���ͷŻ����յ�������Ϊ�÷�Ӧ���¶��µ�...
�����Ȼ�ѧ�еķ�Ӧ���ȣ� ��ѧ��Ӧ���ʱ䣺��ѧ��Ӧ���������ͷŻ����յ�����������...
1������ʲô����ʲô�����йأ����ʵľ�����ֵ�Ƿ�ɲ⣿ ��(����H)��һ������˵���...
��ѧ��ѧ��һ��ʹ�ü���������(ͼ1)���Եزⶨǿ�ᡢǿ����кͷ�Ӧʱ����ЧӦ����...
����ͨ���л�ѧ�γ̱�(ʵ��)���жԻ�ѧ�������ܵ�ת����ѧϰĿ�����������Ҫ��ͨ��...