在中学阶段,对化学知识的学习,一般只注重定性,造成学生缺乏了“量”的意识,因而对许多问题总是含糊不清,或是只知其然而不知其所以然。下面略举几种情况,以期起到抛砖引玉的作用。
1.学习物质的检验和性质要有“量”的意识。如:
(1)在进行物质的检验、鉴别、鉴定、推断时,要“取少量(或适量)……于……中”,否则就意味着是“原瓶操作”;
(2)检验Fe2+、Fe3+有多种方法,但当溶液中Fe2+、Fe3+的浓度很小,或含有大量的其他干扰离子时,就不宜用沉淀法,宜用加入KSCN溶液显色法;
(3)NH3(或NH4+)有多种检验方法,但当NH3的含量(或浓度)很小时,就不宜用指示剂法、沉淀法、白烟法等,宜用倒扣水中溶解观察气体体积变化法;
(4)NH3和HCl均极易溶于水,可用于喷泉实验或会发生倒吸,但当混合气体中NH3或HCl的含量(或浓度)很小时,则未必可形成喷泉或发生倒吸;
(5)SO2、NO2也可形成喷泉或会发生倒吸,但当玻璃管较长时则未必;
(6)具有特征现象的化学反应,仅一个甚至上百个反应物微粒是不能表现出反应现象的,只有当反应物达到了一定量,才能表现出明显的反应现象。
2.判断离子共存要有“量”的意识。如:
(1)H+、NO3-、Fe2+不能大量共存,但却存在Fe(NO3)2溶液(同时含有H+、NO3-、Fe2+),即三者也有共存的“量”的范围;
(2)经判断已洗净的BaSO4沉淀中,是否一定不含有Cl-等离子呢?
3.进行化学实验要有“量”的意识。如:
(1)取用药品不宜过多,以免造成浪费甚至发生危险;
(2)测定中和热所用酸碱溶液的浓度及其体积不宜过大或过小;
(3)做银镜反应实验时,所配置的银氨溶液一定要稀;
(4)做乙醛与氢氧化铜悬浊液反应实验时,所需氢氧化钠溶液和硫酸铜溶液的浓度与用量,以及加入乙醛溶液的体积都有限定,否则将不会产生所需要的现象;
(5)提纯物质时,所加除杂试剂要稍过量。
4.使用一些化学仪器及用品要有“量”的意识。如:
(1)各种容器所盛装试剂的量都有一定的限量范围;
(2)各种测量仪器(如量筒、天平、滴定管、温度计)和用品(如pH试纸)都有一定的测量范围和精确度。
5.使用一定浓度的溶液要有“量”的意识。如:
(1)澄清石灰水。由于Ca(OH)2的溶解度较小,即使饱和的Ca(OH)2溶液也是很稀的溶液,故它只用来检验CO2等气体,不用于吸收CO2。同理,将一定量CO2与HCl的化合气体,依次通过盛有澄清石灰水和Ba(OH)2溶液的洗气瓶,会出现前者无现象后者变浑浊,但若依次通过盛有Ba(OH)2溶液和澄清石灰水的洗气瓶,则可能出现相反的结果;
(2)饱和Na2CO3及NaHCO3溶液。实验室收集乙酸乙酯选用饱和Na2CO3溶液,而不用NaOH溶液或饱和NaHCO3溶液,是因为NaOH溶液易使酯发生水解,NaHCO3的溶解度较小,饱和NaHCO3溶液较稀,吸收乙酸的效果不如饱和Na2CO3溶液,而且乙酸乙酯的溶解度较在饱和Na2CO3溶液中的大;
(3)浓溴水与稀溴水。溴水的颜色与溴水的浓度有关,由稀到浓,溴水的颜色由黄到橙到棕。在检验SO2、CH2=CH2、HC≡CH等气体时,宜用稀溴水。在检验苯酚时要用浓溴水且要过量。
6.比较溶液中粒子浓度的大小要有“量”的意识。如:
Na2CO3溶液中,由于CO32-的水解,使c(Na+)>2c(CO32-)。又CO32-的水解是微弱的,故c(Na+)只是稍大于2c(CO32-)。由CO32-+H2O HCO3-+OH-知,c(HCO3-)=c(OH-),但由于HCO3-+H2O
HCO3-+OH-知,c(HCO3-)=c(OH-),但由于HCO3-+H2O H2CO3+OH-,而使HCO3-有所减少,OH-有所增多,同时OH-还有部分来自H2O的电离,故c(OH-)>c(HCO3-),而且只是稍大于。因为Na2CO3溶液呈碱性,故c(OH-)>c(H+)。由于饱和Na2CO3溶液的pH≈12,则c(OH-)≈1010×c(H+),故c(OH-)>>c(H+),自然c(HCO3-)>c(H+)。因为CO32-的水解是微弱的,故c(CO32-)>>c(OH-)。故有:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)。
H2CO3+OH-,而使HCO3-有所减少,OH-有所增多,同时OH-还有部分来自H2O的电离,故c(OH-)>c(HCO3-),而且只是稍大于。因为Na2CO3溶液呈碱性,故c(OH-)>c(H+)。由于饱和Na2CO3溶液的pH≈12,则c(OH-)≈1010×c(H+),故c(OH-)>>c(H+),自然c(HCO3-)>c(H+)。因为CO32-的水解是微弱的,故c(CO32-)>>c(OH-)。故有:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)。
7.判断分散系中分散质微粒直径的大小要有“量”的意识。如:
分子中含有五十多个碳原子的天然油脂,不属于高分子化合物,淀粉属于高分子化合物,淀粉溶液又属于胶体。可知,1molFeCl3完全水解形成Fe(OH)3胶体微粒的数目,远远小于1NA(NA表示阿伏伽德罗常数)。
8.学习化学平衡要有“量”的意识。
(1)决定可逆过程向某方向进行程度的是物质的本性(内因),而不是外界条件(外因)。如:
①SO2催化氧化反应的转化率本来就较大,改变外界条件也不会有大的改变(不可能达到100%,故无需高压);而合成氨反应的转化率本来就很小,改变外界条件虽也不会有大的改变,但这点不大的改变已可能是原来的数倍,已经相当可观;
②NH3+H2O NH3·H2O的进行程度,远远大于Cl2+H2O
NH3·H2O的进行程度,远远大于Cl2+H2O HCl+HClO,故氨水以NH3·H2O为主,氯水以Cl2为主。
HCl+HClO,故氨水以NH3·H2O为主,氯水以Cl2为主。
(2)改变条件使平衡发生移动,结果只是对改变予以减弱,不会带来大的变化。即增大(或减小)某种量,平衡发生移动后,这种量仍然大(或小),只是在增大(或减小)后被减小(或增大)了些。
另外,可燃性气体的爆炸极限、定量实验中的误差分析、用极限思维解题等,都是学习中学化学中具有“量”的意识的体现。
有了“量”的意识,可使思维更严密,分析更科学,结果更精确。
练习:
1.下列实验中,所加物质的浓度不会影响实验现象的是( )
A.向Fe(OH)3胶体中滴加HCl,先出现沉淀,后沉淀溶解
B.向少量苯酚溶液中滴入溴水,有白色沉淀产生
C.向盛有少量MnO2的烧瓶中加入盐酸,加热,有黄绿色气体产生
D.向盛有少量铜片的试管中加入H2SO4,加热,有气体放出
2.某溶液中存在的离子有S2-、HS-、OH-、Na+、H+。下列对该溶液的有关叙述正确的是( )
A.溶液中一定是:c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+)
B.组成该溶液的溶质只能是Na2S或NaHS或两者的混合物
C.该溶液只能是碱性或酸性
D.加水稀释,溶液中c(H+)可能增大,也可能减小或不变
3.下列实验操作中一定会造成误差的是( )
A.在中和热的测定实验中用Ba(OH)2代替NaOH;H2SO4代替HCl
B.将pH试纸用蒸馏水湿润后测某溶液的pH
C.酸碱中和滴定实验中达到滴定终点后立即读数
D.使用天平称量时不小心将药品与砝码的位置放反了
4.在室温下进行中和滴定,酸和碱恰好完全反应时,以下说法一定正确的是( )
A.参加反应的酸和碱的物质的量相等
B.参加反应的酸中的H+离子总量和碱中OH-离子总量相等
C.反应后混合液的pH=7
D.不能用适当的酸碱指示剂来判断
5.实验室可以用以下两种方案来制取铜粉:
I.Zn+2HCI=ZnCl2+H2↑ CuO+H2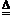 Cu+H2O
Cu+H2O
Ⅱ.CuO+2HCl==CuCl2+H2O CuCl2+Zn=Cu+ZnCl2
下列有关说法正确的是( )
A.制备等量的Cu,需要消耗等量的Zn
B.制备等量的Cu,需要消耗等量的CuO
C.制备等量的Cu,需要消耗等量的HCI
D.制备等量的Cu,生成等量的ZnCl2
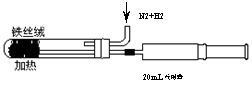
6.如图是实验室模拟工业法合成氨的简易装置。检验有氨气生成的方法是: 。
7.在一定温度下,向一定容积的密闭容器中充入2molA和1molB,发生反应:
2A(g)+B(g)  3C(g);∆H=-a kJ/mol(a>0)
3C(g);∆H=-a kJ/mol(a>0)
达到平衡时放出了b kJ的热量。若向该容器中充入3molC,达到平衡时吸收了c kJ的热量。则a、b、c之间的关系为(用含a、b、c的代数式表示): 。
参考答案:1.A 2.D 3.A 4.D 5.B 6.将注射器取下置于盛水的水槽中,若水进入注射器,气体体积减少,则说明有氨气生成。 7.a=b+c。
(责任编辑:化学自习室)




 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。