
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
![]()
下几种方法:
(1)向可溶性铝盐溶液滴加适量的强碱溶液或稍过量的氨水,其离子方程式分别为:
Al3++3OH-=Al(OH)3↓
![]()
如果向铝盐溶液滴加过量的强碱溶液,就会使Al(OH)3溶解,而转化为偏铝酸盐:
![]()
从实验情况来看,加入强碱溶液来制取Al(OH)3,在操作上是难于控制适量的。因此采用加稍过量氨水的方法是较适宜的,这是由于Al(OH)3是不溶于氨水的。
(2)向可溶性偏铝酸盐溶液滴加适量的强酸溶液或通入稍过量的CO2,其离子方程式分别为:
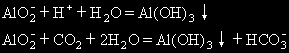
如果向偏铝酸盐溶液滴加过量的强酸溶液,就会使Al(OH)3溶解而转化为铝盐:
Al(OH)3+3H+=Al3++3H2O
从实验情况来看,加入强酸溶液来制取Al(OH)3,在操作上也是难于控制适量。因此采用通入过量的CO2的方法是较适宜的。这是因为Al(OH)3不能溶于碳酸。由此可以得出结论,Al(OH)3的两性只能溶于强酸或强碱溶液,即难溶于弱酸或弱碱溶液。
(3)制取Al(OH)3也可采用把铝盐溶液加入偏铝酸盐溶液的方法,其化学方程式为:
AlCl3+3NaAlO2+6H2O=4Al(OH)3↓+3NaCl
虽然本知识内容教材中没有要求掌握,但是这里提出供学生自学使用,既开宽了学生知识视野,也为高三化学盐的水解学习打好一定的基础。
总结上述几种方面的分析,可将Al(OH)3的制备归纳如下:
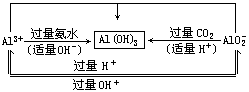

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。化学计算是化学学习中的重点,也是难点。中学化学常见的计算主要分为两个方面:①涉及...
Fe 3+ 有较强的氧化性,可以把铁粉氧化成 Fe 2+ : 2Fe 3+ +Fe=3Fe 2+ ① 这是铁离子...
在涉及金属铝及其化合物的计算中,有一类重要的计算,就是铝盐溶液与强碱溶液、偏铝酸...
1、何为过量? 如某反应中两种反应物的量都已给出,则应先通过计算判断两种反应物是否...
铁与稀硝酸的反应与反应物的量有关,原因在于金属铁有变价。具体情况比较复杂,归纳解...
一、问题的提出 将amolFe 3+ 、bmolCu 2+ 、cmolFe和dmolCu混合于同一反应体系(溶液...