
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、概述
氧化铝(Al₂O₃)晶体既不是纯粹的离子晶体,也不是纯粹的共价晶体,而是离子键与共价键之间的过渡晶体(混合型晶体)。
键型特征:Al³⁺与O²⁻之间的化学键具有显著的共价性,离子键成分约为40%–50%(不同计算方法略有差异),因此更偏向于共价键主导。
结构与性质:常见晶型(如α-Al₂O₃,刚玉)中,Al与O通过强共价键形成三维网状结构,表现为高熔点、高硬度、不溶于水和一般酸碱,这些性质更接近共价晶体。
教学处理:在部分教材中,基于键型百分比和物理性质,常将Al₂O₃当作共价晶体处理,但需理解其本质为过渡晶体。
二、争论与分析:
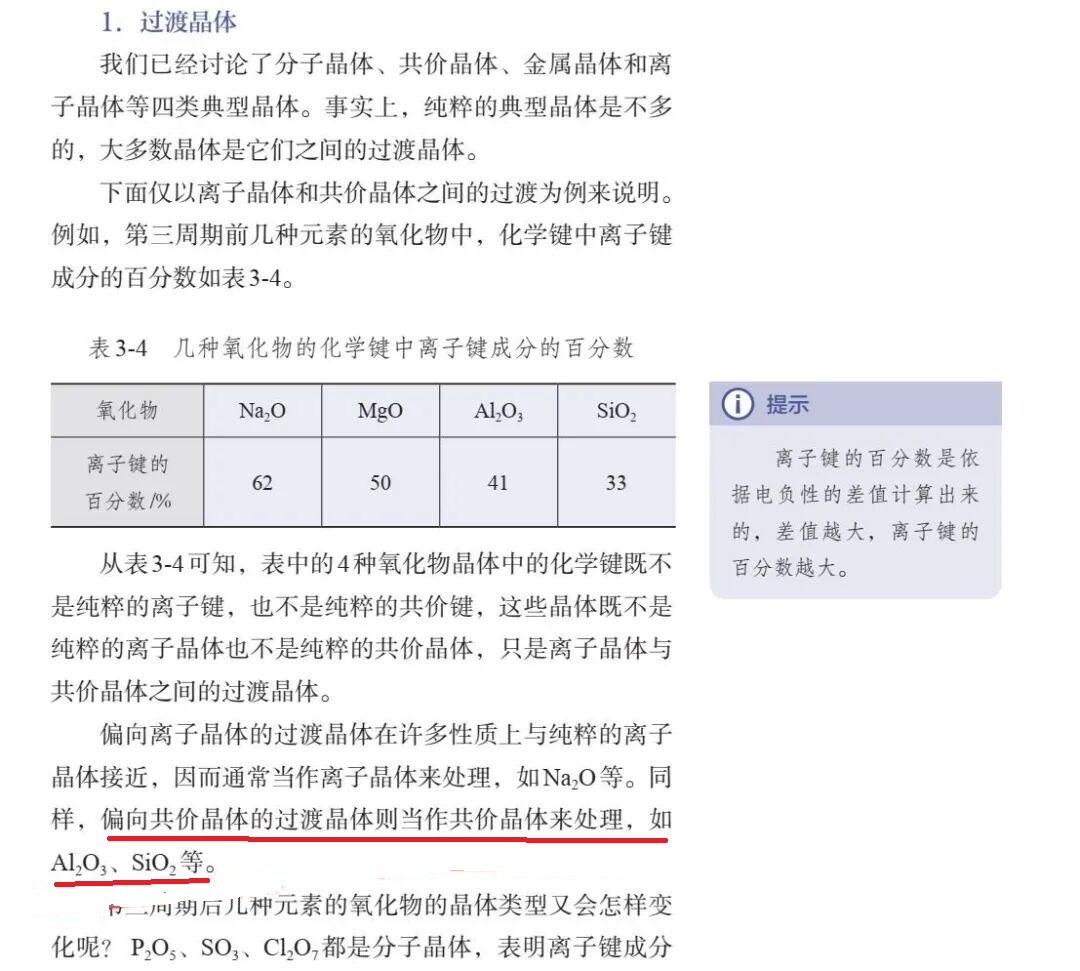
很长一段历史时期内,高中阶段都深信不疑氧化铝属于离子化合物。而且经常被拿出来与工业不能用电解氯化铝的方法做比对。人教版最新版显示氧化铝离子键百分比为41%,显然按这个数据键型偏共价键更多一些,所以归为共价晶体处理。
但是这个离子键百分比咋搞出来的?是否具有权威性?大家是否公认呢?我们来看一下几种计算键型百分比的方法:
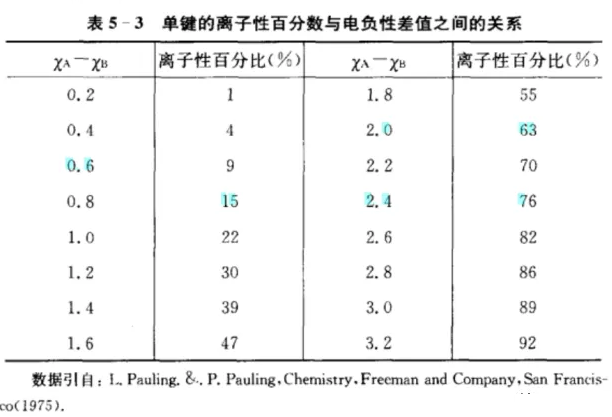




根据上述资料,有很多所谓“经验性公式”计算键型百分比。有些权威教授自己也有弄经验公式的。有的资料(结晶化学导论)号称利用公式fi=C²/(Eh²+C²)可以精确计算离子键成分。我用好几个“经验性”公式计算发现Al₂O₃离子键百分比从46%~63%不等,没有查询到氧化铝的共价能带间隙和离子能带间隙,所以没有用“精确公式”做计算。但是,根据结晶化学导论,离子键和共价键键型转变的转折点是六配位变为四配位。那么我们就从配位数及键长角度做一下分析。请看下列资料:
统计结果见下表:
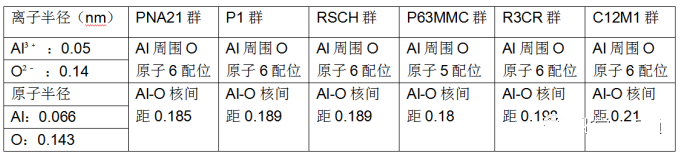
根据上表,Al³⁺与O²⁻半径之和为0.05+0.14=0.19,与PNA21、P1、RSCH、P63MMC这几种空间群非常接近。Al原子与O原子半径之和为0.066+0.143=0.209,与R3CR、C12M1这两种空间群很接近。
我们知道离子键没有方向性和饱和性,所以离子键典型结构就是在离子周围尽可能多的吸引异性离子。铝是ⅢA主族,价电子为3如果形成共价键如果不考虑配位键那么仅能形成3个共价键,配位数应该是3。
所以无论从配位数看,还是从氧铝核间距与二者离子半径、原子半径之和的关系看。
大部分晶型的氧化铝应该是离子晶体更靠谱一些,从配位数看P63MMC群晶型可能更接近共价晶体,从核间距看R3CR与C12M1群晶型可能更偏向共价晶体。
总结:根据上述资料分析,我认为根据“经验性”公式计算得离子键百分比并不很靠谱,计算结果也只能仅作参考。因为这些公式绝大部分是根据电负性搞出来的,而电负性有很多不同标准,这些不同标准有的甚至相差较大。综合考虑配位数、核间距等因素,
我认为大部分晶型的氧化铝离子键成分应该更高一些。所以对于氧化铝的晶体类型最好应该模糊处理,鲁科版、沪教版、苏教版对此都没有做出明确说明,人教版明确氧化铝属于共价晶体应该不是很科学。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
一、为什么“摩擦”能加快结晶? 你可以把溶液里的溶质分子想...
一、物质的聚集状态的存在形式 1.通常物质有三态:固态、液...
物质熔点越高,沸点一定也越高吗? 答:不一定。熔点强调的是...
在常见元素中,硼注定是那特别的一个——价层电子只有3个,却...
...
...