
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
高考答题存在的主要问题有:
1.不会根据物质的性质选择分离提纯的方法,对有机物分离提纯常用方法的原理和仪器不是很熟悉;
2.有机物制备实验题的答题思路还需要进一步总结;
3.实验现象的描述不够“精准”;
4.做计算题的信心不足,有效数字存在一些问题。
高考化学有机实验题的基本流程和注意事项
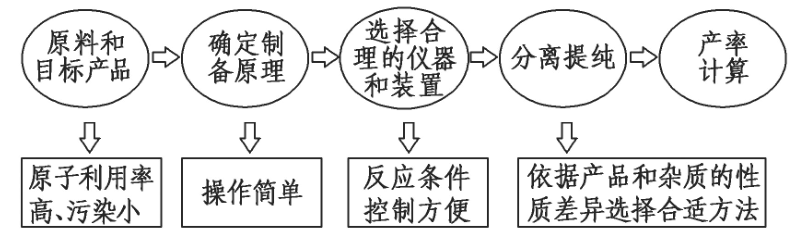
有机物制备实验的基本模型是反应原理的选择、装置的选择、实验操作的步骤、杂质的分析、产物的分离与提纯、产率的计算等。每一阶段的问题总是围绕着原料经济、操作简单、产量更高、纯度更好的目的展开。
答题关键:获取信息,根据信息选择装置和分离提纯的方法,将信息与问题“对号入座”。有机物制备中一般会给出相应的信息,通常会以表格的形式给出,表格中的数据主要是有机化合物的密度、沸点和在水中的溶解性,在分析这些数据时要多进行横向和纵向地比较,密度主要是与水比较,沸点主要是表中各物质的比较,溶解性主要是判断溶还是不溶。主要是根据这些数据选择分离、提纯的方法。
一、典型基本流程:
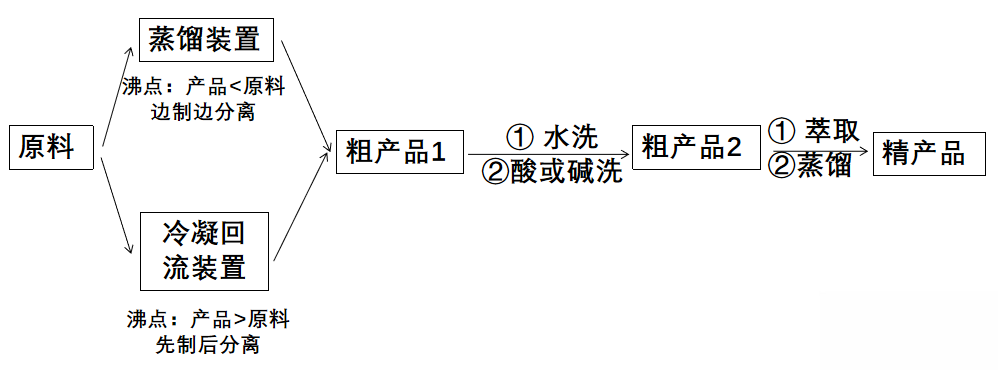
答题关键:根据沸点、溶解性、密度等信息选择分离提纯的方法。获取信息,将信息与问题“对号入座”
二、有机实验要注意安全,有机物常易燃易爆
实验操作主要考虑实验安全、实验效果和干扰因素的排除和控制,经常考的实验操作有:试剂混合顺序、加热方式、操作顺序、沸石的作用、事故的处理等。
1.若用到浓硫酸,其加入顺序如何?
先加水(或其他如乙醇等),再滴加浓硫酸(有时还要边加边搅拌),因为浓硫酸溶于水会放出大量热,容易溅出伤人。
2.有机物制备实验应注意的安全事项有什么?
防暴沸(加沸石、搅拌磁子)防爆炸(如控温)、防倒吸(如制溴苯、制乙酸乙酯)、
3.安全瓶的作用?
安全瓶:防止倒吸;检查实验进行时管路是否发生堵塞。如下图装置,若堵塞,现象是:B中水面下降,玻璃管(即安全管)中水柱上升,甚至溢出。
安全管的作用是什么?防止某容器中压强过大。(见2017国Ⅰ第26题)
4.若有机产品易被氧化,如何防止其被氧化?
例如:使用加水稀释浓硫酸,降低浓硫酸浓度以减少副产物的生成。
5.加入浓硫酸并不断搅拌的目的是什么?
例如:搅拌防止局部过热;混匀,防止局部炭化;防止某些试剂结块等。
6.减压蒸馏的目的是什么?
在较低温度下蒸馏出产品,避免产品因温度高而分解或被氧化等。
7.如何处理尾气?
(1)如甲烷、乙烯、乙炔的制取实验中可将可燃性的尾气燃烧掉
(2)溴苯的制取实验、硝基苯的制备实验中可用冷却的方法将有害挥发物回流
三、有机溶剂一般易挥发,需冷凝、回流等装置
1.若有机反应物易挥发,应采取什么措施?
例如:冷凝回流(用长玻璃管或冷凝管等);
例如:用到浓硫酸的反应,讲浓硫酸适当稀释可以减少其他反应物的挥发。
有时候长导管的作用只是冷凝而不回流,如制乙酸乙酯。
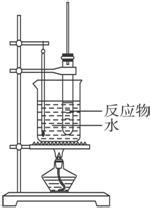
制硝基苯时长导管作用:冷凝回流
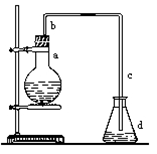
制溴苯时长直导管b的作用:导气、冷凝回流
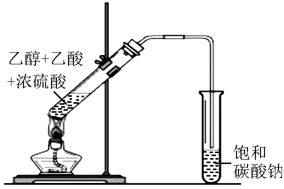
长导管的作用:导气、将反应生成的乙酸乙酯蒸气冷凝
2.注意冷却:
有机实验中的反应物和产物多为挥发性的有害物质,所以必须注意对挥发出的反应物和产物进行冷却。这些实验需要冷却的目的是减少反应物或生成物的挥发,既保证了实验的顺利进行,又减少了这些挥发物对人的危害和对环境的污染
(1)需要冷水(用冷凝管盛装)冷却的实验:蒸馏水的制取实验、石油的蒸馏实验
(2)用空气冷却(用长玻璃管连接反应装置)的实验:硝基苯的制取实验、酚醛树酯的制取实验、乙酸乙酯的制取实验、石蜡的催化裂化实验、溴苯的制取实验
四、根据物质和反应特点,确定实验仪器和装置
1.制备装置中常用的仪器有哪些?
例如: 四种冷凝管:直形冷凝管、球形冷凝管、空气冷凝管、蛇形冷凝管。
|
|
|
a为直形冷凝管。用于蒸馏,便于液体冷凝后流出
b为球形冷凝管。一般用于反应装置,防止易挥发物质蒸发流失,起冷凝回流的作用
c为空气冷凝管,当蒸馏物沸点超过140摄氏度时,一般使用空气冷凝管,以免直形冷凝管通水冷却导致玻璃温差大而炸裂
d为蛇形冷凝管。主要用于冷凝收集沸点偏低蒸馏产物
四种烧瓶:
|
|
三颈烧瓶(三个口可变换着插入分液漏斗、温度计、搅拌器、冷凝管、滴液漏斗等) |
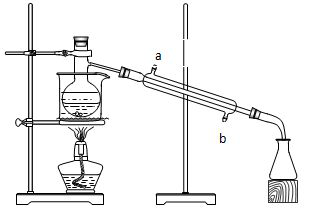
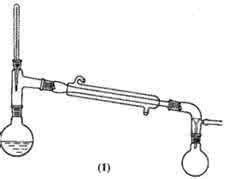
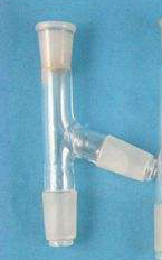
圆底烧瓶加个蒸馏头,就可以用来蒸馏啦!
五种漏斗:
|
|
|
|
|
普通漏斗 | 长颈漏斗 | (用于分液) | (用于滴加反应液) | 恒压滴液漏斗(支管的作用是平衡压强,使漏斗内液体顺利流下) |
2.加热的方式有哪些?
(1)酒精灯加热。
酒精灯的火焰温度一般在 400~500℃,所以需要温度不太高的实验都可用酒精灯加热。教材中用酒精灯加热的有机实验是:乙烯的制备实验、乙酸乙酯的制取实验、蒸馏石油实验、石蜡的催化裂化实验
(2)酒精喷灯加热。
酒精喷灯的火焰温度比酒精灯的火焰温度要高得多,所以需要较高温度的有机实验可采用酒精喷灯加热。教材中用酒精喷灯加热的有机实验是:煤的干馏实验
(3)水浴加热。
水浴加热的温度不超过 100℃。教材中用水浴加热的有机实验有:银镜实验(包括醛类、糖类等的所有的银镜实验)、硝基苯的制取实验(水浴温度为 60℃)、酚醛树酯的制取实验(沸水浴)、乙酸乙酯的水解实验(水浴温度为 70℃~80℃)、糖类(包括二糖、淀粉和纤维素等)水解实验(热水浴)
水浴加热的优点是:①反应器受热均匀;②便于控制温度不高于 100℃;③可避免由于反应物沸点低受热时未参加反应即脱离反应混合体系
(4)用温度计测温的有机实验有:
硝基苯的制取实验、乙酸乙酯的制取实验(以上两个实验中的温度计水银球都是插在反应液外的水浴液中,测定水浴的温度)、乙烯的实验室制取实验(温度计水银球插入反应液中,测定反应液的温度)、石油的蒸馏实验(温度计水银球应插在具支烧瓶支管口处,测定馏出物的温度)
五、有机反应一般为可逆反应,要采取措施使平衡向右移动,提高产品的产率
1.有机反应一般是可逆的,采取什么条件可以使平衡向右移动,提高产品的产率?
例如:增大某反应物的浓度(往往是廉价的那一种)、及时分离出产物(如酯的制备用分水器及时分离出水)
例如:采用边反应边蒸出产物的方式,使产品馏出,离开体系。
2.是否所有有机反应都可以边反应边蒸馏出产品? 否。
若产品的沸点低于原料的沸点:可边反应边蒸馏,可用如下装置:
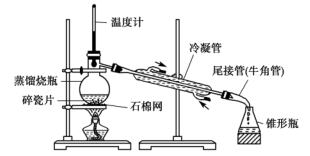
若产品的沸点高于原料的沸点,可用冷凝回流装置,可用如下装置:
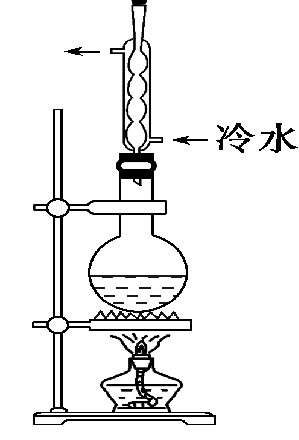
六、有机反应通常副反应多、副产物多,产品需要提纯。
混合物 | 试剂 | 方法 |
乙烷(乙烯) | 溴水 | 洗气 |
乙炔(硫化氢) | CuSO4 溶液或 NaOH 溶液 | |
乙酸乙酯(乙酸) | 饱和 Na2CO3 溶液 | 分液 |
溴苯(溴) | NaOH 溶液 | |
硝基苯(硝酸、硫酸) | NaOH 溶液 | |
苯(苯甲酸) | NaOH 溶液 | |
苯(苯酚) | NaOH 溶液 | |
苯(甲苯) | 酸性 KMnO4 溶液 | |
乙醇(水) | CaO | 蒸馏 |
乙醇(乙酸) | NaOH 溶液 | |
粗苯甲酸 |
此外还有过滤、萃取、盐析、渗析、结晶、升华、色谱等方法,据混合物性质而定
1.操作的考查:
蒸馏操作的注意事项有哪些?苯甲酸重结晶的操作步骤是什么?分液漏斗使用的注意事项有哪些?
2.杂质的来源有哪些?
①残留的反应物(一般不能进行完全)②主反应的副产物③副反应的产物④催化剂及沸石⑤反应所需的溶剂
3.有机产品杂质的一般步骤是什么?
例如:水洗、盐洗(或酸碱洗)、水洗、干燥(如加入无水CaCl2、MgSO4等)、过滤除去干燥剂、蒸馏;或萃取、分液、重结晶。
4.两次水洗的目的分别是什么?
第一次水洗洗去大部分可溶性杂质第二次水洗洗去上一步加入的过量的洗涤试剂。
5.如何检验晶体产品已经洗涤完全?
[答题模板] 取少许最后一次洗涤滤液于试管中,滴加 少量×××溶液,若出现×××现象,则表明沉淀已洗。(“取加若则”)
以洗去Cl-为例:答:取最后一次的洗涤液少量于试管中,滴入1~2滴稀硝酸,再滴加1~2滴AgNO3溶液,若无白色沉淀生成,则说明沉淀已经洗涤干净,若出现白色沉淀则表明沉淀未洗净。(严格按照“操作(实验步骤)+现象+结论”的格式叙述。)
6.为什么有时用饱和食盐水洗涤有机产品?
可降低有机物在水中的溶解度,减少洗涤时有机物的损失。
【解题技巧】
把所需要的反应产物与杂质分离开来,这就需要根据各组分物理常数的差异,选择适当的混合物分离技术。
如气体产物中的杂质,一般可通过装有液体或固体吸收剂的装置除去;液体产物可借助萃取或蒸馏的方法进行纯化;不互溶的用分液,互溶的用蒸馏。
固体产物则可利用沉淀分离、重结晶或升华的方法进行精制。有时还可以通过离子交换或色层分离的方法来达到纯化物质的目的。
七、有机物一般在水中的溶解度较小,易溶于有机溶剂。
注意答题过程中注意挖掘提干提供的信息(溶解度、密度等)、用信息,答案往往隐藏在信息中。
【解题技巧】陌生有机物的溶解度等相关物理性质,题中一般都会给出数据,抓住这些数据的应用会给解题带来很大的方便。如相对分子质量会在计算是用到,密度会在分层时判断有机物所在用到,溶解度会在溶解、萃取、结晶和洗涤时用到,熔沸点会在控温和蒸馏时用到。
在分析这些数据时要多进行横向和纵向地比较,密度主要是与水比较,沸点主要是表中各物质的比较,溶解性主要是判断溶还是不溶。根据这些数据选择分离、提纯的方法。
八、产率、纯度、质量分数等定量计算

总结:有机物制备实验题答题思路

有机物制备实验的基本模型是反应原理的选择、装置的装配、实验操作的步骤、杂质的分析、产物的分离与提纯、产率的计算等。每一阶段的问题总是围绕着原料经济、操作简单、产量更高、纯度更好的目的展开。有了这个模型,就能将具体的问题套入相应的模型中,就能看清问题的本质,具体明确地回答各种问题。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
【导读】卤代烃鉴定先酸化后加银,蔗糖水解先碱化后检验醛基...
...
...
名称 索氏提取器 仪器 主要 用途 索氏提取器就是利用溶剂回流...
在乙酸乙酯的制备实验中,乙醇、乙酸、浓硫酸加入顺序人教版...
“有机实验”在高考中频频出现,主要涉及有机物的制备、有机...