
|
学习小专题 |
 过氧化钠相关计算的八个推论
日期:2022-01-13 20:07:22
点击:1363
好评:0
过氧化钠相关计算的八个推论
日期:2022-01-13 20:07:22
点击:1363
好评:0
过氧化钠的 相关计算题涉及的解题技巧和方法较多,对于初学者而言难度较大,甚至让很多学生深深感到头疼。 为了帮 助高一学生度过过氧化钠计算难关,现整理出与过氧化钠计算相关的八条重要推论 。 一.过氧化钠与二氧化碳的反应 先请同学们根据过氧化钠与二氧化碳反应的...
 课堂实录之高中化学通:氧化钠和过氧化钠的性质
日期:2018-07-17 11:21:32
点击:263
好评:0
课堂实录之高中化学通:氧化钠和过氧化钠的性质
日期:2018-07-17 11:21:32
点击:263
好评:0
课堂实录之高中学习帮:氧化钠和过氧化钠的性质...
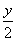 二氧化碳水与足量过氧化钠的反应规律
日期:2016-01-18 14:08:26
点击:9940
好评:0
二氧化碳水与足量过氧化钠的反应规律
日期:2016-01-18 14:08:26
点击:9940
好评:0
1、分别写出由CO 2 、H 2 O与足量Na 2 O 2 的反应的化学方程式,并写出每1mol CO 2 和每 1mol H 2 O与足量Na 2 O 2 完全反应后,Na 2 O 2 增重的质量: CO 2 +Na 2 O 2 = 与足量的Na 2 O 2 反应,Na 2 O 2 增重 g。 1mol CO 2 H 2 O +Na 2 O 2 = 与足量的Na 2 O 2 反应...
 过氧化钠生成的演示实验
日期:2016-01-18 10:55:55
点击:11892
好评:0
过氧化钠生成的演示实验
日期:2016-01-18 10:55:55
点击:11892
好评:0
高中化学课本中关于钠在空气里燃烧生成过氧化钠的实验,只有“把小块钠放在石棉网上加热,观察发生的变化。”一句,给人的印象是,这个实验非常简单,然而事实上远非如此轻而易举。我们曾按课本所述方法反复实验,终未能如愿。尽管也偶尔发现燃烧产物表面好象略显淡黄色...
 趣味实验-吹气生火
日期:2011-12-13 09:52:55
点击:4671
好评:0
趣味实验-吹气生火
日期:2011-12-13 09:52:55
点击:4671
好评:0
实验原理 过氧化钠能与二氧化碳反应产生氧气并放出大量的热,使棉花着火燃烧。 实验用品 蒸发皿、玻璃棒、镊子、细长玻璃管。 Na2O2、脱脂棉。 实验步骤 1.把少量Na2O2粉末平铺在一薄层脱脂棉上,用玻璃棒轻轻压拨,使Na2O2进入脱脂棉中。 2.用镊子将带有Na2O2的脱脂棉轻轻卷...
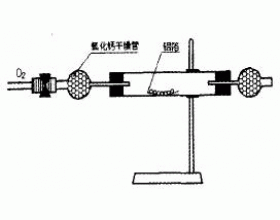 如何使钠的燃烧产物显淡黄色?
日期:2011-12-13 08:31:24
点击:7794
好评:0
如何使钠的燃烧产物显淡黄色?
日期:2011-12-13 08:31:24
点击:7794
好评:0
在金属的化学性质的教学中,金属钠的化学性质中安排了钠在空气中的燃烧实验,目的是观察钠的颜色反应和燃烧产物过氧化钠的颜色和状态。教材中是在燃烧匙内进行该实验的,由于燃烧匙凹陷、且暴露在空气中,得到的通常是灰色糊状物质,学生很难观察到过氧化钠淡黄色颗粒状现象...
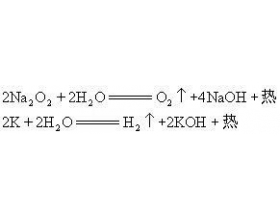 趣味实验-冰棍点烟
日期:2011-08-31 10:15:27
点击:3351
好评:0
趣味实验-冰棍点烟
日期:2011-08-31 10:15:27
点击:3351
好评:0
一、实验原理 由于香烟上的Na 2 O 2 (或钾)与冰棍接触,它们很快与冰棍上的水作用。发生的化学反应如下: 反应生成了氧气,并放出大量热,所以使香烟点着。 二、实验用品 香烟、Na 2 O 2 粉末、金属钾、冰棍。 三、实验操作 在香烟一头撒上少量干燥的黄色过氧化钠(Na 2 O...
 过氧化钠在离子方程式中要拆开吗?
日期:2011-08-30 12:44:12
点击:6560
好评:0
过氧化钠在离子方程式中要拆开吗?
日期:2011-08-30 12:44:12
点击:6560
好评:0
在水溶液中不能拆,因为固体的Na2O2中过氧根离子不能自由移动,所以不能拆,但在水溶液中没过氧根离子,过氧根离子遇水马上反应生成OH-和O2,所以就不存在过氧根离子在水溶液里,所以不能拆。但在熔融状态,没有水,Na2O2能电离出过氧根离子.完全电离.所以要拆.初中高中一般不讲熔融...
 有强氧化性的物质为什么就可以做漂白剂?
日期:2010-07-28 16:07:51
点击:4569
好评:4
有强氧化性的物质为什么就可以做漂白剂?
日期:2010-07-28 16:07:51
点击:4569
好评:4
1、漂白是和有机物起反应而使其褪色。 2、有机物是含碳的化合物,有颜色的有机物一般都具有复杂的结构,其中一般含各种环,含有个数不等的双键,故一般都能够被氧化。 3、具有强氧化性的物质可以将有色的有机物氧化,将其原有结构破坏,而又不使其碳化,从而不再具有原来的颜色...
 二氧化硫与过氧化钠反应生成什么?
日期:2008-03-03 11:38:34
点击:5597
好评:2
二氧化硫与过氧化钠反应生成什么?
日期:2008-03-03 11:38:34
点击:5597
好评:2
实验于下: 实验 1 集满一瓶 SO 2 ,用镊子或坩锅钳夹取一团包有 Na 2 O 2 粉末的棉花团伸入瓶中,棉团立即着火燃烧 ( 当心集气瓶破裂 ) 且反应比在 CO 2 中迅猛。 如果说 SO 2 与 Na 2 O 2 的反应按下式进行: Na 2 O 2 +SO 2 =Na 2 SO 4 +Q, 反应放出的热量多,温度...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。