
|
学习小专题 |

|
学习小专题 |
 [方法与规律k] 有关电化学的计算模式 作者:王辉 来源:未知 日期:2016-02-03 14:42:10 点击:8106 所属专题:电化学计算
[方法与规律k] 有关电化学的计算模式 作者:王辉 来源:未知 日期:2016-02-03 14:42:10 点击:8106 所属专题:电化学计算
一、根据相应的电化学方程式进行计算 (基本模式) 如:用惰性电极电解氯化钠溶液 2NaOH + 2H 2 O H 2 ↑ + 2NaOH + Cl 2 ↑∽ 2e - 80g 2mol 22.4L 2mol 22.4L 2N A m(g) x(mol) V(L) z(mol) V (L) N(个) 然后根据已知和未知条件列比例求解。 二、根据电极反应试进...
 [方法与规律k] 电极反应式书写方法 作者:李萍 来源:未知 日期:2013-02-27 19:31:36 点击:9597 所属专题:电极反应式
[方法与规律k] 电极反应式书写方法 作者:李萍 来源:未知 日期:2013-02-27 19:31:36 点击:9597 所属专题:电极反应式
电极反应书写的思路 1、先写出电极主要反应物和和主要产物; 2、由化合价写出得失电子数: 3、由电荷守恒写出箭头左边或右边相应的离子; 4、由质量守恒配平电极反应。 例题1:已知高铁电池的总反应为 3 z N+2Na 2 FeO 4 +8H 2 O 3 z n (OH) 2 +2Fe(OH) 3 +4NaOH 充电时...
 [方法与规律k] 化学电极判断分析 作者:田兴虎 来源:未知 日期:2021-12-21 11:49:15 点击:11019 所属专题:电极判断
[方法与规律k] 化学电极判断分析 作者:田兴虎 来源:未知 日期:2021-12-21 11:49:15 点击:11019 所属专题:电极判断
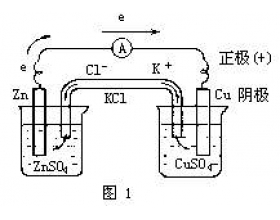
有学生问:正(+)极是不是阳极,负(-)极是不是阴极;-、+与阴、阳是否都对应;一会儿负极发生氧化反应,正极发生还原反应,一会儿又是阴(-)极发生还原反应,这是怎么回事?有人认为,“阴极发生还原反应,阳极发生氧化反应”的说法是决不会有错,这又是怎么回事?就我所...
 [方法与规律k] 用石墨电解CuSO4的和NaCl混合液的pH变化 作者:爱莉 来源:未知 日期:2012-10-22 11:01:09 点击:4326 所属专题:连续电解
[方法与规律k] 用石墨电解CuSO4的和NaCl混合液的pH变化 作者:爱莉 来源:未知 日期:2012-10-22 11:01:09 点击:4326 所属专题:连续电解
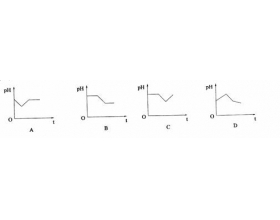
先看原题:将等物质的量浓度CuSO 4 的和NaCl溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液PH随时间t变化走势为: 答案为:D 解析:等物质的量浓度CuSO 4 的和NaCl溶液等体积混合,可以设CuSO 4 的和NaCl各1mol, 电解分3个阶段: 第一阶段 阳极:1mol氯离子失1mo...
 [方法与规律k] 图解电化学的程序分析法 作者:黄增春 来源:未知 日期:2014-12-18 10:52:35 点击:3203 所属专题:电化学
[方法与规律k] 图解电化学的程序分析法 作者:黄增春 来源:未知 日期:2014-12-18 10:52:35 点击:3203 所属专题:电化学
电化学中的电极反应比较复杂,既要考虑阳极、阴极、正极、负极的性质,又要考虑电解质溶液中阴离子的还原性强弱和阳离子的氧化性强弱, 为了便于学生解题,特图解电化学的程序分析。希望对学生和老师有所帮助。...
 [方法与规律k] 高中化学中电化学的程序分析法 作者:刘洪林 来源:未知 日期:2013-03-07 16:14:52 点击:4285 所属专题:电化学
[方法与规律k] 高中化学中电化学的程序分析法 作者:刘洪林 来源:未知 日期:2013-03-07 16:14:52 点击:4285 所属专题:电化学
电化学中的电极反应比较复杂,既要考虑阳极、阴极、正极、负极的性质,又要考虑电解质溶液中阴离子的还原性强弱和阳离子的氧化性强弱,为了便于学生解题,特图解电化学的程序分析。希望对学生和老师有所帮助。...
 [方法与规律k] 电镀池的规律 作者:许雁祥 来源:未知 日期:2012-05-21 11:01:36 点击:3992 所属专题:电镀
[方法与规律k] 电镀池的规律 作者:许雁祥 来源:未知 日期:2012-05-21 11:01:36 点击:3992 所属专题:电镀
以镀层金属为阳极,待镀金属制品为阴极,含镀层金属离子的溶液为电镀液。 电镀过程的特点:①牺牲阳极;②电镀液的浓度(严格说是镀层金属离子的浓度)保持不变;③在电镀控制的条件下,水电离产生的H + 、OH - 一般不放电。...
 [方法与规律k] 电解基本规律 作者:董啸 来源:未知 日期:2012-05-21 10:55:46 点击:7251 所属专题:电解规律
[方法与规律k] 电解基本规律 作者:董啸 来源:未知 日期:2012-05-21 10:55:46 点击:7251 所属专题:电解规律
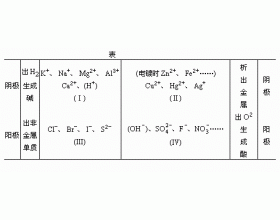
各离子放电情况分析表 1.各类电解质溶液的电解情况分析 若溶液中阳离子仅有(Ⅰ)中或类似的离子,则通电后逸出H 2 ,生成对应碱。 若溶液中阳离子只要有(Ⅱ)的离子,则通电后析出金属单质。 若溶液中阴离子只要有(Ⅲ)的离子,则通电后析出非金属单质。 若溶液中阴离子...
 [方法与规律k] 电解后的溶液复原例析 作者:栾春武 来源:未知 日期:2019-06-28 18:41:11 点击:22450 所属专题:溶液复原
[方法与规律k] 电解后的溶液复原例析 作者:栾春武 来源:未知 日期:2019-06-28 18:41:11 点击:22450 所属专题:溶液复原
一、知识点 电解质溶液进行电解时,大致分三种情况,①电解质本身被电解,②溶剂水被电解,③电解质和水同时被电解。因此要使电解后的溶液恢复原状,必须根据电解的化学反应原理来确定。同学们可记为:出去什么就加什么。 ①电解质本身被电解,如电解 HCl溶液:2HCl H 2...
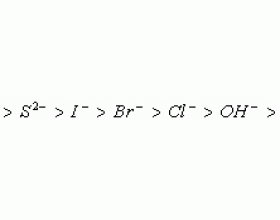 [方法与规律k] 电解知识点及应用 作者:何清松 来源:未知 日期:2012-03-26 22:38:20 点击:10566 所属专题:电解池
[方法与规律k] 电解知识点及应用 作者:何清松 来源:未知 日期:2012-03-26 22:38:20 点击:10566 所属专题:电解池
一. 基本知识点 1. 电解池: 将电能转化为化学能的装置。它由三部分组成,一是外接直流电源,二是阴阳两极,三是电解质溶液。 2. 电解池中的反应 与电源正极相连的电极为阳极,发生氧化反应;与电源负极相连的电极为阴极,发生还原反应。 要正确地判断和书写两极的电极反应...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。电化学原理是普通高中化学选择性必修1化学反应原理中的重要组成部分,也是高考化学中...
一、判断有机物得失电子 例1: 微生物电池是指在微生物的作用下将化学能转化为电能的...
近几年全国卷高考电化学装置一般都带有离子交换膜,此类题目新颖度高,学生因理不清交...
【 知识归纳 】 1. 浓差电池的定义 物质由 高浓度 向 低浓度 扩散而引发的一类电池称...
锌溴液流电池是一种大规模储能电池,相比传统铅酸电池锂离子电池等,把电解质存放在容...
11111...
1.纯水体系或强酸强碱形成的正盐溶液(如NaCl) 此时溶液中的H+完全由水电离,则C 平 ...
【 知识归纳 】 1 .离子交换膜的功能 使离子选择性定向迁移 ( 目的是平衡整个溶液的...