
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
1.锂离子电池
锂系电池分为锂电池和锂离子电池。手机和笔记本电脑使用的都是锂离子电池,通常人们俗称其为锂电池。电池一般采用含有锂元素的材料作为电极,是现代高性能电池的代表。而真正的锂电池由于危险性大,很少应用于日常电子产品。
锂离子电池由日本索尼公司于1990年最先开发成功。它是把锂离子嵌入碳(石油焦炭和石墨)中形成负极(传统锂电池用锂或锂合金作负极)。正极材料常用LixCoO2,也用LixNiO2,和LixMnO4,电解液用LiPF6+二乙烯碳酸酯(EC)+二甲基碳酸酯(DMC)。
石油焦炭和石墨作负极材料无毒,且资源充足,锂离子嵌入碳中,克服了锂的高活性,解决了传统锂电池存在的安全问题,正极LixCoO2在充、放电性能和寿命上均能达到较高水平,使成本降低,总之锂离子电池的综合性能提高了。预计21世纪锂离子电池将会占有很大的市场。
锂离子电池是一种二次电池(充电电池),它主要依靠锂离子在正极和负极之间移动来工作。在充放电过程中,Li+在两个电极之间往返嵌入和脱嵌:充电时,Li+从正极脱嵌,经过电解质嵌入负极,负极处于富锂状态;放电时则相反。
2.锂离子电池的组成结构
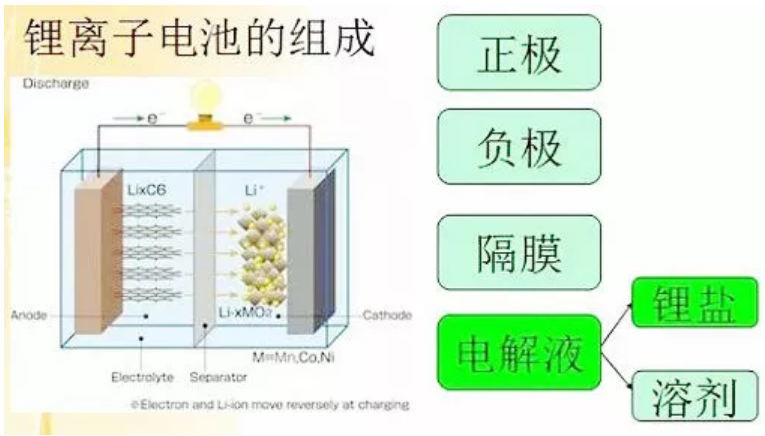
钢壳/铝壳/圆柱/软包装系列:
(1)正极——活性物质一般为锰酸锂或者钴酸锂,镍钴锰酸锂材料,电动自行车则普遍用镍钴锰酸锂(俗称三元)或者三元+少量锰酸锂,纯的锰酸锂和磷酸铁锂则由于体积大、性能不好或成本高而逐渐淡出。导电极流体使用厚度10--20微米的电解铝箔。
(2)隔膜——一种经特殊成型的高分子薄膜,薄膜有微孔结构,可以让锂离子自由通过,而电子不能通过。
(3)负极——活性物质为石墨,或近似石墨结构的碳,导电集流体使用厚度7-15微米的电解铜箔。
(4)有机电解液——溶解有六氟磷酸锂的碳酸酯类溶剂,聚合物的则使用凝胶状电解液。
(5)电池外壳——分为钢壳(方型很少使用)、铝壳、镀镍铁壳(圆柱电池使用)、铝塑膜(软包装)等,还有电池的盖帽,也是电池的正负极引出端。
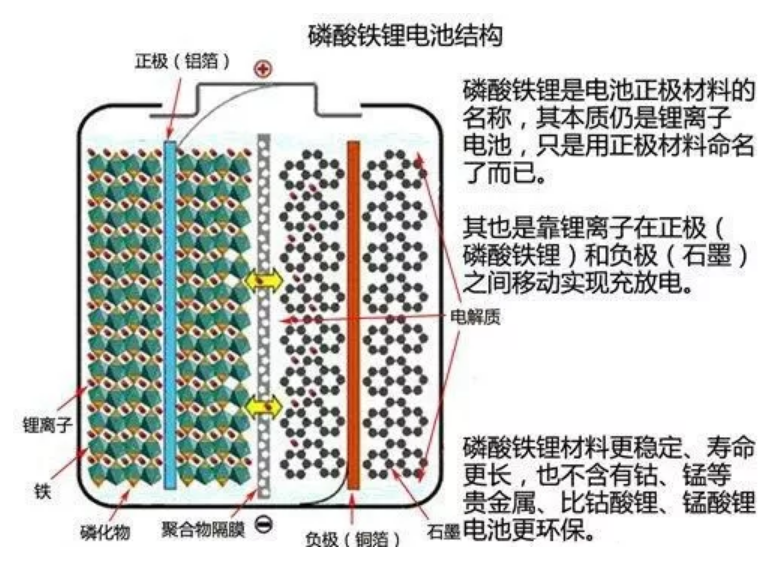
3.制作工艺:
锂电池的正极材料有钴酸锂LiCoO2、三元材料Ni+Mn+Co、锰酸锂LiMn2O4加导电剂和粘合剂,涂在铝箔上形成正极,负极是层状石墨加导电剂及粘合剂涂在铜箔基带上,比较先进的负极层状石墨颗粒已采用纳米碳。
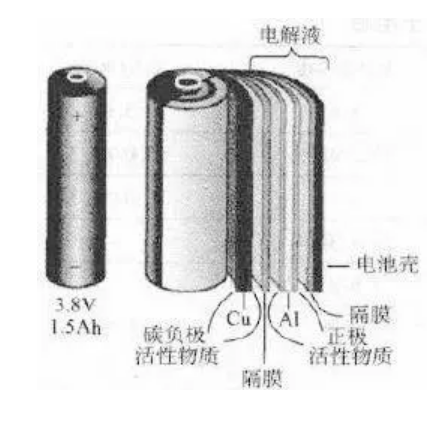
(1)制浆:用专门的溶剂和粘结剂分别与粉末状的正负极活性物质混合,经搅拌均匀后,制成浆状的正负极物质。
(2)涂膜:通过自动涂布机将正负极浆料分别均匀地涂覆在金属箔表面,经自动烘干后自动剪切制成正负极极片。
(3)装配:按正极片—隔膜—负极片—隔膜自上而下的顺序经卷绕注入电解液、封口、正负极耳焊接等工艺过程,即完成电池的装配过程,制成成品电池。
(4)化成:将成品电池放置测试柜进行充放电测试,筛选出合格的成品电池,待出厂。
4.锂离子电池的工作原理
锂离子电池以碳素材料为负极,以含锂的化合物作正极,没有金属锂存在,只有锂离子。锂离子电池是指以锂离子嵌入化合物为正极材料电池的总称。锂离子电池的充放电过程,就是锂离子的嵌入和脱嵌过程。在锂离子的嵌入和脱嵌过程中,同时伴随着与锂离子等当量电子的嵌入和脱嵌(习惯上正极用嵌入或脱嵌表示,而负极用插入或脱插表示)。在充放电过程中,锂离子在正、负极之间往返嵌入/脱嵌和插入/脱插,被形象地称为“摇椅电池”。
当对电池进行充电时,电池的正极上有锂离子生成,生成的锂离子经过电解液运动到负极。而作为负极的碳呈层状结构,它有很多微孔,达到负极的锂离子就嵌入到碳层的微孔中,嵌入的锂离子越多,充电容量越高。同样,当对电池进行放电时(即我们使用电池的过程),嵌在负极碳层中的锂离子脱出,又运动回正极。回正极的锂离子越多,放电容量越高。
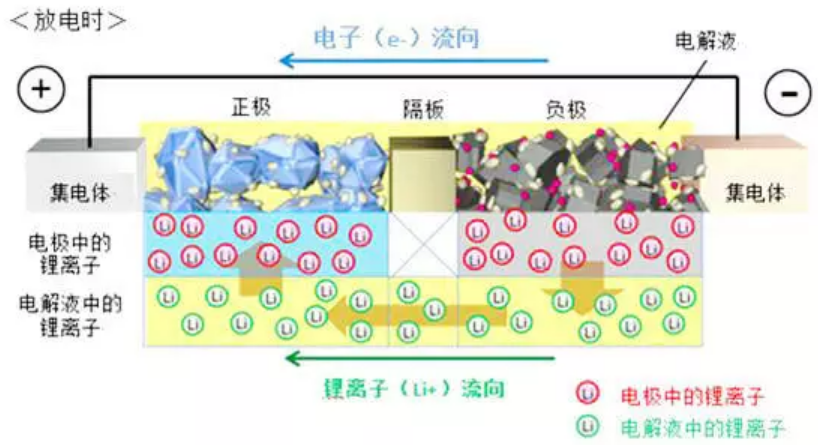
下图是英文图注的锂离子电池工作原理图,如果你英文不好,却能够看懂,说明你对锂离子电池的工作原理基本掌握了。
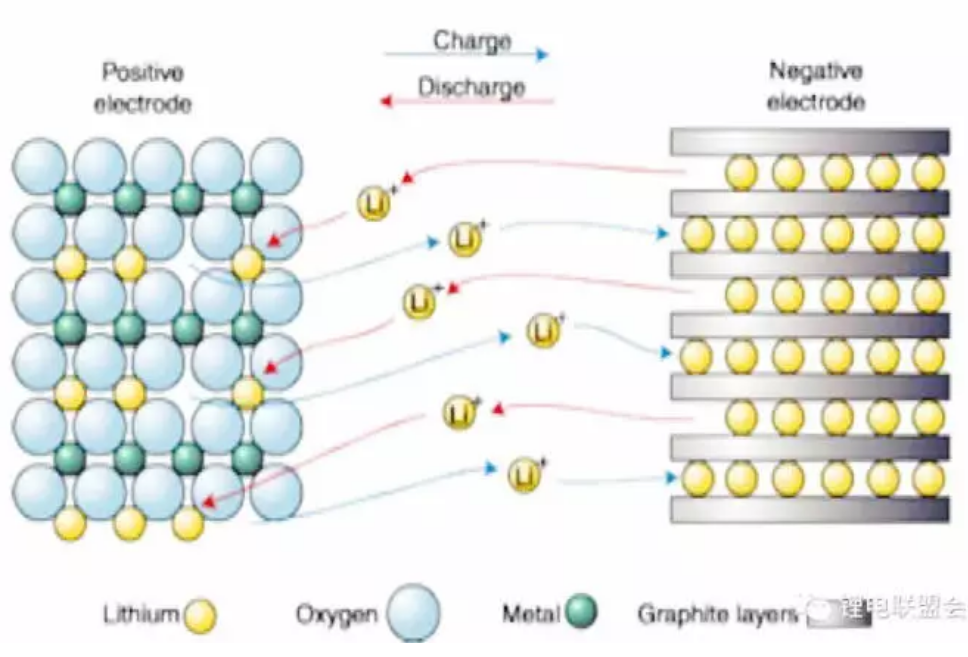
一般锂电池充电电流设定在0.2C至1C之间,电流越大,充电越快,同时电池发热也越大。而且,过大的电流充电,容量不够满,因为电池内部的电化学反应需要时间。就跟倒啤酒一样,倒太快的话会产生泡沫,反而不满。
以磷酸亚铁锂为例,其放电和充电时的电极反应分别为:
正极反应:
充电时锂离子脱嵌:LiFePO4→Li1-xFePO4+xLi++ xe-
放电时锂离子嵌入:Li1-xFePO4+xLi++ xe-→LiFePO4
负极反应:
充电时锂离子插入:xLi++ x e-+ 6C →LixC6
放电时锂离子脱插:LixC6→ xLi++ x e-+ 6C
以钴酸锂作为正极材料的锂离子电池,其充电和放电的电极反应为:
充电时的反应式:LiCoO2+C→Li1-xCoO2+LixC
放电时的反应式为:Li1-xCoO2+LixC→LiCoO2+C
事实上,正极材料中的CoO2-和FePO4-在电池中作为类似“骨架”而使得Li+得以在其中自由的移动,负极材料的石墨碳能够亲和Li+而使得Li的活性变得温和而持续。
5.锂离子手机电池爆炸的原因分析
电池充电时发生爆炸的主要原因有两个,一是过热,二是短路。而短路形成的主要原因是电池的隔膜过薄或质量存在问题,在充电时形成的金属锂形成结晶刺破隔膜导致短路。所以使用手机时应该注意以下问题:
(1)防摔:手机摔落可以改变电池的内部机械或化学结构。这些变化可能导致任何故障安全电路在极端压力条件下发生故障。
(2)避免过热:虽然电池中可能存在保护措施以确保其散热,或者在过热时关闭,但首先要保持电池远离温度限制。防止过热的方法是,避免长时间使用,并且不要暴晒电池或讲电池至于温度较高的环境中。
(3)使用安全的充电器:一定要使用电池生产厂提供的充电器。过高的充电电压、过高的充电电流都会造成电池的损害。
(4)防水:电池掉入水中是很危险的,一定要注意避免。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
锂离子蓄电池,负极材料是石墨,负极的充电反应为: xLi + +...
...
锂离子电池是二次可充放电电池,核心工作逻辑是锂离子的嵌脱...
在高考化学电化学模块中,带离子交换膜的电化学装置是绝对高...
锌溴液流电池是一种大规模储能电池,相比传统铅酸电池锂离子...
【解析】: A.电解氧化的目的是在铝制品表面形成氧化膜,所以代...