
|
学习小专题 |
 在金属活动性顺序里为什么包括氢
日期:2022-08-12 07:42:03
点击:7739
好评:0
在金属活动性顺序里为什么包括氢
日期:2022-08-12 07:42:03
点击:7739
好评:0
1865年,贝开托夫(Бекетов)在实验的基础上,根据金属和金属离子间互相置换能力的大小,以及金属跟酸、跟水等反应的剧烈程度,首先确定了金属活动性顺序,在这个顺序里就已包括了氢。因为氢可以被位于它前面的金属从稀酸里置换出来,而氢也右以把位于它后面的金...
 完整版金属活动性表
日期:2020-04-08 22:25:56
点击:11494
好评:0
完整版金属活动性表
日期:2020-04-08 22:25:56
点击:11494
好评:0
Li K Rb Cs Ra Ba Sr Ca Na Ac La Ce Pr Nd Pm Sm Eu 锂、钾、铷、铯、镭、钡、锶、钙、钠、锕、镧、铈、镨、钕、钷、钐、铕、 Gd Tb Y Mg Am Dy Ho Er Tm Lu(H) Sc Pu Th Np Be 钆、铽、钇、镁、镅、镝、钬、铒、铥、镥、(氢)、钪、钚、钍、镎、铍、 U Hf Al Ti Zr V...
 在金属活动顺序表中,Ca位于Na的前面,为什么钙与水反应不如钠与
日期:2017-04-17 14:59:30
点击:1509
好评:0
在金属活动顺序表中,Ca位于Na的前面,为什么钙与水反应不如钠与
日期:2017-04-17 14:59:30
点击:1509
好评:0
在金属活动顺序表中,Ca位于Na的前面,应该像钠一 样与水反应,且比钠与水反应剧烈,但由于生成Ca(OH) 2 微溶,易沉积在钙的表面,阻碍了钙与水的进一步反应,因而钙与水反应不如钠与水反应剧烈。...
 使用金属活动性顺序表应注意几点
日期:2016-04-21 11:53:09
点击:6605
好评:2
使用金属活动性顺序表应注意几点
日期:2016-04-21 11:53:09
点击:6605
好评:2
经过长期的实践,人们总结出常见金属活动 性顺序如下: K Ca Na Mg Al Zn Fe Sn Pb( H) Cu Hg Ag Pt Au 金属活动性由强逐渐减弱 并习惯称其为金属活动性顺序表。 初中教材中对金属活动性顺序的叙述是“在 金属活动性顺序中,金属的位置越靠前,金属在水 溶液中就越容易失去...
 金属活动性顺序中的第二条泾渭分明线
日期:2016-01-18 17:55:32
点击:10966
好评:1
金属活动性顺序中的第二条泾渭分明线
日期:2016-01-18 17:55:32
点击:10966
好评:1
金属活动性顺序中的第一条分界线就是众所周知的(H)所处的位置,在它的左侧金属单质能与盐酸、稀硫酸等发生置换反应,生成盐和氢气;而在位于(H)右侧的金属单质则不能发生这类反应。 那么金属活动性顺序中的第二条分界线在什么位置?别急! 先把Ba 放在金属活动性顺序中C...
 金属活动顺序表的涵义
日期:2016-01-18 16:29:41
点击:14422
好评:0
金属活动顺序表的涵义
日期:2016-01-18 16:29:41
点击:14422
好评:0
金属活动顺序 K Ca Na Mg Al Mn Zn Cr Fe Ni Sn Pb H Cu Hg Ag Pt Au 原子失电子(还原性)能力 由 强 到 弱 离子得电子(氧化性)能力 由 弱 到 强 与氧气反应 常温易氧化 常温可氧化 加热时可被氧化 不能氧化 与水作用 与冷水剧烈 反 应 与沸水缓慢反应 高温水蒸气 不能...
 金属活动顺序表的应用
日期:2016-01-18 16:29:01
点击:17773
好评:0
金属活动顺序表的应用
日期:2016-01-18 16:29:01
点击:17773
好评:0
常见金属的活动顺序为: K 、 Ca 、 Na 、 Mg 、 Al 、 Zn 、 Fe 、 Sn 、 Pb(H) 、 Cu 、 Hg 、 Ag 、 Pt 、 Au ,从左右顺序,反映了金属在溶液中失电子生成金属阳离子的能力逐渐减弱 ( 即还原性 ) ,而其对应的阳离子得电子能力逐渐增强 ( 即氧化性 ) 。 该表有多种...
 金属活动顺序表的八大用途
日期:2016-01-18 16:27:33
点击:23503
好评:0
金属活动顺序表的八大用途
日期:2016-01-18 16:27:33
点击:23503
好评:0
金属活动顺序表是学好中学化学(包括高中化学)的重要工具。它在初中化学中有着广泛的用途,下面从八个方面对金属活动顺序表在初中化学中的用途进行总结。 1. 用于确定金属单质能否与酸发生置换反应 金属与酸的置换反应是初中化学的重要反应,哪些金属能与什么样的酸发生...
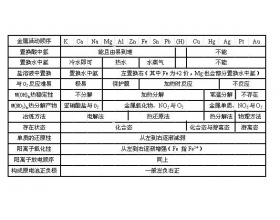 金属活动顺序及其应用一览表
日期:2016-01-18 16:18:19
点击:3622
好评:0
金属活动顺序及其应用一览表
日期:2016-01-18 16:18:19
点击:3622
好评:0
...
 能否用金属与酸反应的快慢描述金属活动性顺序?
日期:2015-01-12 15:05:55
点击:7219
好评:0
能否用金属与酸反应的快慢描述金属活动性顺序?
日期:2015-01-12 15:05:55
点击:7219
好评:0
例如,铝与稀硫酸的反应是金属与酸的重要反应。我们将已除去氧化膜的等体积、大小形状相同的铝片和铁片分别与稀硫酸反应,实验发现,铁片与稀硫酸反应时,铁片表面有较多气泡生成,而铝片与硫酸的反应,只是开始时有极少量气泡产生,但很快便会中止。若金属与酸反应的快...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。