
|
学习小专题 |
 恒温下向醋酸钠稀溶液中加入少量固体醋酸钠,醋酸根离子与钠离子
日期:2025-07-29 15:57:16
点击:1388
好评:0
恒温下向醋酸钠稀溶液中加入少量固体醋酸钠,醋酸根离子与钠离子
日期:2025-07-29 15:57:16
点击:1388
好评:0
请教:恒温下向CH 3 COONa稀溶液中加入少量固体醋酸钠 c (CH 3 COO - )/ c (Na + )比值增大吗? 一般讲离子浓度比值的题都用极限法。比如这个题,开始醋酸根比钠离子比值是小于一的,后来加入醋酸钠固体,如果加了无限多的醋酸钠,这个体系就变成醋酸钠了。那么离子浓...
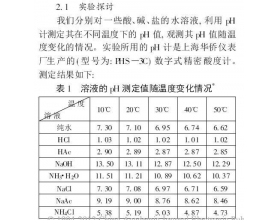 强碱弱酸盐的pH一定随温度升高而增大吗?
日期:2021-12-02 10:42:42
点击:2835
好评:0
强碱弱酸盐的pH一定随温度升高而增大吗?
日期:2021-12-02 10:42:42
点击:2835
好评:0
...
 通俗讲义:水解反应及其原理
日期:2020-03-05 11:16:22
点击:20087
好评:1
通俗讲义:水解反应及其原理
日期:2020-03-05 11:16:22
点击:20087
好评:1
一.水解的前提 水解反应首先是将水分子一解为二,否则水解无从谈起。 H-OH被解离成H原子和-OH,或H + 和OH - 。 不可能解离成O原子。那不是水解,那是电解。 水解主体亦一解为二,并选择性结合H或OH。 二.从“没的挑”到“有的挑” 很熟悉Cl 2 与H 2 O的反应。 Cl 2 +...
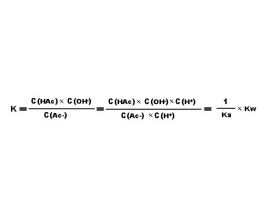 水解平衡常数的计算
日期:2019-11-24 16:15:21
点击:138219
好评:9
水解平衡常数的计算
日期:2019-11-24 16:15:21
点击:138219
好评:9
一.醋酸钠溶液的水解(强碱弱酸盐水解) Ac - +H 2 O HAc+OH - 平衡常数 : (Kw 是水的离子积, Ka 是醋酸的电离常数 ) 二.氯化铵溶液的水解(强酸弱碱盐水解) NH4++H2ONH3.H2O+H+ 平衡常数 : (Kw 是水的离子积, Kb 是氨水的电离常数 ) 三.醋酸铵溶液的水解(弱酸弱...
 微课视频:盐类水解原理与规律
日期:2017-05-31 14:58:29
点击:419
好评:0
微课视频:盐类水解原理与规律
日期:2017-05-31 14:58:29
点击:419
好评:0
微课视频:盐类水解原理与规律...
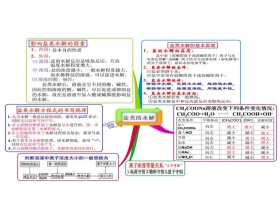 盐类的水解之思维导图
日期:2016-12-19 10:44:06
点击:6645
好评:0
盐类的水解之思维导图
日期:2016-12-19 10:44:06
点击:6645
好评:0
...
 盐类水解学习中的几个误区
日期:2016-05-12 19:17:28
点击:1048
好评:0
盐类水解学习中的几个误区
日期:2016-05-12 19:17:28
点击:1048
好评:0
...
 课件学习:盐类的水解
日期:2012-11-27 18:23:59
点击:404
好评:0
课件学习:盐类的水解
日期:2012-11-27 18:23:59
点击:404
好评:0
...
 实验模拟:盐溶液的pH值检验
日期:2012-11-27 18:17:32
点击:371
好评:0
实验模拟:盐溶液的pH值检验
日期:2012-11-27 18:17:32
点击:371
好评:0
...
 课件学习:盐类的水解
日期:2012-04-24 22:09:26
点击:371
好评:0
课件学习:盐类的水解
日期:2012-04-24 22:09:26
点击:371
好评:0
...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。