
|
学习小专题 |
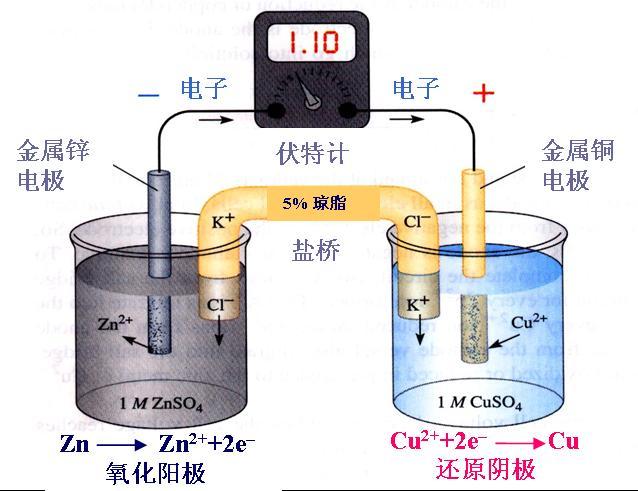
 高中常见的原电池电极反应式的书写
日期:2018-03-14 16:44:58
点击:7873
好评:0
高中常见的原电池电极反应式的书写
日期:2018-03-14 16:44:58
点击:7873
好评:0
一次电池 1、伏打电池:(负极—Zn、正极—Cu、电解液—H 2 SO 4 ) 负极:Zn-2e - ==Zn 2+ (氧化反应) 正极: 2H + +2e - ==H 2 ↑(还原反应) 总反应Zn + 2H + == H 2 ↑+ Zn 2 + 2、铁碳电池:(负极—Fe、正极—C、电解液H 2 CO 3 弱酸性) 负极:Fe-2e - ==Fe ...
 注重解题程序 、正确书写燃料电池的电极反应式
日期:2017-04-25 20:09:38
点击:1145
好评:0
注重解题程序 、正确书写燃料电池的电极反应式
日期:2017-04-25 20:09:38
点击:1145
好评:0
一、电极反应书写常见错误举例及错因分析 1.完成甲烷—硫酸构成的燃料电池的电极反应 1正极:2O 2 +8e - +4H + =4OH - 2正极:O 2 +8e - =O 2- 3正极:2O 2 +8e - +4H 2 O=8OH - 4负极:CH 4 -8e - +2OH - =CO 2 +6H 2 O 5正极:CH 4 -8e - +3OH - =C O 3 2 ...
 几种常见的“燃料电池”的电极反应式的书写
日期:2017-04-25 19:56:12
点击:42816
好评:7
几种常见的“燃料电池”的电极反应式的书写
日期:2017-04-25 19:56:12
点击:42816
好评:7
燃料电池是原电池中一种比较特殊的电池,它与原电池形成条件有一点相悖,就是不一定两极是两根活动性不同的电极,也可以用相同的两根电极。燃料电池有很多,下面主要介绍几种常见的燃料电池,希望达到举一反三的目的。 一、氢氧燃料电池 氢氧燃料电池一般是以惰性金属铂...
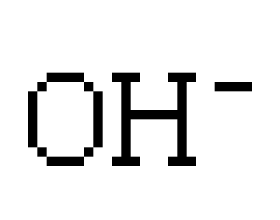 常见的原电池电极反应式书写汇总
日期:2017-04-25 17:33:40
点击:64369
好评:0
常见的原电池电极反应式书写汇总
日期:2017-04-25 17:33:40
点击:64369
好评:0
一次电池 1 、伏打电池: (负极 —Zn 、正极 —Cu 、电解液 —H 2 SO 4 ) 负极: Zn–2e - ==Zn 2+ ( 氧化反应 ) 正极: 2H + +2e - ==H 2 ↑( 还原反应 ) 离子方程式 Zn+2H + ==H 2 ↑+Zn 2+ 2 、铁碳电池: (负极 —Fe 、正极 —C 、电解液 H 2 CO 3 弱酸性 ) 负极...
 书写电极反应的四原则
日期:2017-04-25 17:32:34
点击:1371
好评:0
书写电极反应的四原则
日期:2017-04-25 17:32:34
点击:1371
好评:0
1.加和性原则:根据得失电子守恒,总反应式为两个反应式之和,若已知一个电极反应式,可用总反应式减去已知的反应式,得另一电极反应式。 2.能否共存原则:因为物质得失电子后在不同的介质环境中所存在的形式不同,所以电极反应式必须考虑介质环境。碱性溶液中CO 2 不...
 燃料电池电极反应式书写经验规则
日期:2017-04-25 17:30:01
点击:1828
好评:0
燃料电池电极反应式书写经验规则
日期:2017-04-25 17:30:01
点击:1828
好评:0
燃料电池的原理: 燃料+O 2 =产物+能量,正极通入的物质均为O 2, 在本质上:正极的电极反应均是O 2 +4e - =O 2- ,而O 2- 的存在与电池的环境有关。 燃料电池有5种: 1酸性燃料电池。 2碱性燃料电池。 3熔融碳酸盐电池。 4熔融氧化物电池。 5质子交换膜电池 我们用...
 有水参与的电极反应式的书写
日期:2016-02-04 13:21:21
点击:6185
好评:0
有水参与的电极反应式的书写
日期:2016-02-04 13:21:21
点击:6185
好评:0
一、问题的提出 现行高中化学教材的各种版本中,有关有水参与电解的电解池离子方程式是这样书写的,以电解饱和食盐水为例: 阳极:2Cl - -2e - =Cl 2 ↑ 阴极:2H + +2e - =H 2 ↑ 总反应的离子方程式为:2Cl - +2H 2 O 2OH - +Cl 2 ↑+H 2 ↑, 化学方程式为...
 燃料电池电极反应式的书写步骤与方法
日期:2014-09-15 11:07:11
点击:2092
好评:0
燃料电池电极反应式的书写步骤与方法
日期:2014-09-15 11:07:11
点击:2092
好评:0
电极:惰性电极;燃料包含:H 2 ;烃如:CH 4 ;醇如:C 2 H 5 OH等。 电解质包含: ①酸性电解质溶液如:H 2 SO 4 溶液; ②碱性电解质溶液如:NaOH溶液; ③熔融氧化物如:Y 2 O 3 ; ④熔融碳酸盐如:K 2 CO 3 等。 第一步:写出电池总反应式 燃料电池的总反应与燃料的燃...
 燃料电池电极反应式的书写应用举例
日期:2014-09-08 11:48:49
点击:1562
好评:0
燃料电池电极反应式的书写应用举例
日期:2014-09-08 11:48:49
点击:1562
好评:0
1、电解质为酸性电解质溶液 例1、科学家预言,燃料电池将是21世纪获得电力的重要途径,美国已计划将甲醇燃料用于军事目的。一种甲醇燃料电池是采用铂或碳化钨作电极催化剂,在稀硫酸电解液中直接加入纯化后的甲醇,同时向一个电极通入空气。 试回答下列问题: ⑴这种电池放...
 常见燃料电池的电极反应式
日期:2014-04-21 10:17:40
点击:300
好评:0
常见燃料电池的电极反应式
日期:2014-04-21 10:17:40
点击:300
好评:0
常见燃料电池的电极反应式...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。