
|
ѧϰСר�� |

|
ѧϰСר�� |
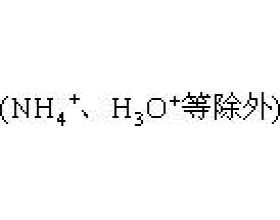 [ע�������a] ����ʽ��д��Ӧ��ע��ļ������� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-08-03 10:35:21 �����1017 ����ר�⣺����ʽ
[ע�������a] ����ʽ��д��Ӧ��ע��ļ������� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-08-03 10:35:21 �����1017 ����ר�⣺����ʽ
����ʽ����Ҫ�Ļ�ѧ���������ر�ʾ��ԭ�ӡ����ӡ����ӻ�������ۻ�����Ľṹ���γɣ�Ҫ����ȷ�����պ�Ӧ�ã���дʱ����ע���������⡣ 1. �õ���ʽ��ʾ���ӻ�������γɵ�ע��� ��1�����д���γ����ӻ������и�ԭ�ӵĵ���ʽ���ұ�д�����ɵ����ӻ�����ĵ���ʽ...
 [ע�������a] �������⻯ѧ���Ķ��壿 ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-07-31 17:32:38 �����1740 ����ר�⣺��ѧ��
[ע�������a] �������⻯ѧ���Ķ��壿 ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-07-31 17:32:38 �����1740 ����ר�⣺��ѧ��
01 ���ڵ�ԭ��֮�� ����ԭ��ָ�����ӻ����ڲ��������ӣ�ԭ�ӻ����ӣ� ���磺HCl�����ڵ�H��Clԭ�ӣ�NaCl�����е������Ӻ������ӡ� 02 ǿ������� �����ڲ���Щ���ڵ�ԭ�Ӵ�������ã����簱����ˮ��HF���ڵ�����������ǻ�ѧ�� һ����Ϊԭ��֮��������ǿ����4...
 [ע�������a] ������������ǿ��˳�� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-07-30 18:42:45 �����11276 ����ר�⣺����
[ע�������a] ������������ǿ��˳�� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-07-30 18:42:45 �����11276 ����ר�⣺����
��ѧ��ѧ���������У�H 2 SiO 3 (ƫ����)�� n (������)��H 2 CO 3 (̼��)��HF(����ᣬ���ټ�)��CH 3 COOH(Ҳ��C 2 H 4 O 2 ���ᣬ�ֽд���)��H 2 S(������)��HClO(������)��HNO 2 (�����ᣬ���ټ�)����ѧ��Χ�ڵ����е��л���(��ѧ��ѧϰ�л�ǿ��)��HNC(����)�ȡ�û������...
 [ע�������a] �������������ص��� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-06-24 17:11:25 �����583 ����ר�⣺���Ӽ�������
[ע�������a] �������������ص��� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-06-24 17:11:25 �����583 ����ר�⣺���Ӽ�������
�������������ص��飺 һ�����Ӽ�: ������Ӽ����ɵ���ת��(ʧȥ������Ϊ�����ӣ���õ�����Ϊ������)�γɵġ��������Ӻ�����֮�����ھ����������γɵĻ�ѧ�������Ӽȿ����ǵ����ӣ���Na �� ��Cl �� ��Ҳ������ԭ�����γɣ���N O 3 �� �ȡ� ���ʣ����Ӽ���������...
 [ע�������a] dz̸�������ȶ��ԵıȽ� ����:������ ��Դ:δ֪ ���ڣ�2022-05-20 09:52:14 �����5712 ����ר�⣺�ȶ���
[ע�������a] dz̸�������ȶ��ԵıȽ� ����:������ ��Դ:δ֪ ���ڣ�2022-05-20 09:52:14 �����5712 ����ר�⣺�ȶ���
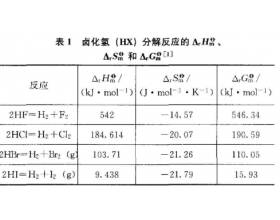
1��������� ���ȶ��������ʵ���Ҫ����֮һ������ѧ�Σ�ͨ��ʵ�������֤�������ȶ��Ե�ǿ����һ���2�����濼�ǣ� һ�ǿ�����ͬ���¶ȣ�ͨ��ʵ������Ƚ����ʷ����ȷֽ����������� ���Dz�������ͬʱ�������ʷ�����ͬ�̶ȵ��ȷֽ�����Ҫ�IJ�ͬ�¶ȡ� 2�ַ������...
 [ע�������a] ����ǽ����Ժͷǽ������ ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-03-03 18:18:47 �����993 ����ר�⣺�ǽ�����
[ע�������a] ����ǽ����Ժͷǽ������ ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-03-03 18:18:47 �����993 ����ר�⣺�ǽ�����
�ǽ�������ָԪ�ص�ԭ�ӵõ����ӵ�������ǿ������Ԫ��ԭ�ӵı������ԡ�����ǿ��ֻ��ԭ�ӽṹ�йأ�������������ء��ǽ��������ָ�ǽ��������ڻ�ѧ��Ӧ�еķ�Ӧ�����Ĵ�...
 [ע�������a] �����������۲쵽С��ԭ������ģ� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-02-08 19:21:35 �����580 ����ר�⣺����
[ע�������a] �����������۲쵽С��ԭ������ģ� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-02-08 19:21:35 �����580 ����ר�⣺����
�ڽ���̫�����ε�ͬʱ������Ҳ��̽���ŷ��ӡ�ԭ��������ԭ�ӻ�С�������档�ڼ��������İ����£��˵���Ұ������С���������������� �š� 17���ͣ����������ĺ������������� ��ѧ���� �۲һ��ˮ�ᄍ����270���С�����ЩС������ٵ��ܶ��š�Ť���š���...
 [ע�������a] ��ˮ����ͨˮ����Щ���� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-02-08 18:35:18 �����1706 ����ר�⣺��ˮ ͬλ��
[ע�������a] ��ˮ����ͨˮ����Щ���� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2022-02-08 18:35:18 �����1706 ����ר�⣺��ˮ ͬλ��
���������϶ȾͻῪʼ�ڻ������Ǵ�Ҷ���Ϥ��֪ʶ��Ȼ���������Ͼ��С��ȱ���������3.8��ſ�ʼ�ڻ����Dz��ǽ�����ֱ���ˮ������?�����ǡ��γ����֡��ȱ�����Ҳ�ǵصص�����ˮ������������ͨˮ��Щ��һ����������ˮ������Է���������18����20�� ��ˮ����Է�������Ϊ...
 [ע�������a] ��ԭ�Ӻ��йصĻ�ѧ֪ʶ ����:������ ��Դ:δ֪ ���ڣ�2021-12-17 10:59:55 �����543 ����ר�⣺ԭ�ӹ���
[ע�������a] ��ԭ�Ӻ��йصĻ�ѧ֪ʶ ����:������ ��Դ:δ֪ ���ڣ�2021-12-17 10:59:55 �����543 ����ר�⣺ԭ�ӹ���
1.���Ӷ���������ɣ�ͬ�Ե������֮����ų⣬Ϊʲô���ǿ��Ծۼ���һ���γ��ȶ���ԭ�Ӻ��أ� ˵����֮�����ų⣬������Ϊ����֮����ڵ���������� ���ǣ���Ȼ�粻ֻ���ڵ��������һ��������������������⣬����ǿ����á�������á��Լ����������� ԭ�Ӻ���...
 [ע�������a] ���ں��������������������ǿ������ ����:������ ��Դ:δ֪ ���ڣ�2021-11-08 09:56:13 �����1237 ����ר�⣺������
[ע�������a] ���ں��������������������ǿ������ ����:������ ��Դ:δ֪ ���ڣ�2021-11-08 09:56:13 �����1237 ����ר�⣺������
�����������е����ǣ������ĺ��������и�ij�ᡢ��ij�ᡢ��ij�ᡢ��ij�ᡢƫij��ȣ���Щ���ƾ����������涨�ģ���ͬԪ�صĺ����ᣬͬ��Ԫ�ز�ͬ��̬�ĺ����ᣬ������ǿ���кι��ɣ�Ϊʲô����������Ҏ�ɣ������������ǿ������ȡ����ʲô�����أ� 1���Ժ��������Ա��ʵķ���...
 ��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ�
��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ� ��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء�
��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء�һ���о���ʷ ��Ȼ�������ʳ����Ĵ�����ʽ����̬��Һ̬��̬����������״̬����Ҫԭ...
...
�������������ͼ��ܵĹ�ϵ�ڻ�ѧ��ͨ������Ϊ���ȹ��ɣ�����Խ�̣�����Խ����ԭ��...
�˽̰���л�ѧ����һ��2019��6�µ�1��2024��7�µ�8��ӡˢP 10 3 ����±�ص�������...
����0�濪ʼ�ڻ������DZ��Ҷ���Ϥ���¶��� Ȼ���������Ͼ����ȱ�����3.8�淽���ڻ�! ...
1. Ϊʲô HF ���Ӽ������ H 2 O ���Ӽ����ǿ���� HF �ķе�ȴ�� H 2 O �ĵͣ� ����...
1��Ϊʲô������û��������ۣ����쳯� ���Ƿǽ�������ǿ��Ԫ�أ�������û��������...
1.���������Ӽ��������ı���Ҳ�Ǿ������ã� ���ȣ��ڼ��Է����뼫�Է���֮�䣬����...