
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
钙钛矿
钙钛矿(CaTiO3)和铁钛矿(FeTiO3)是钛的重要来源。钙钛矿的晶体晶胞如图。
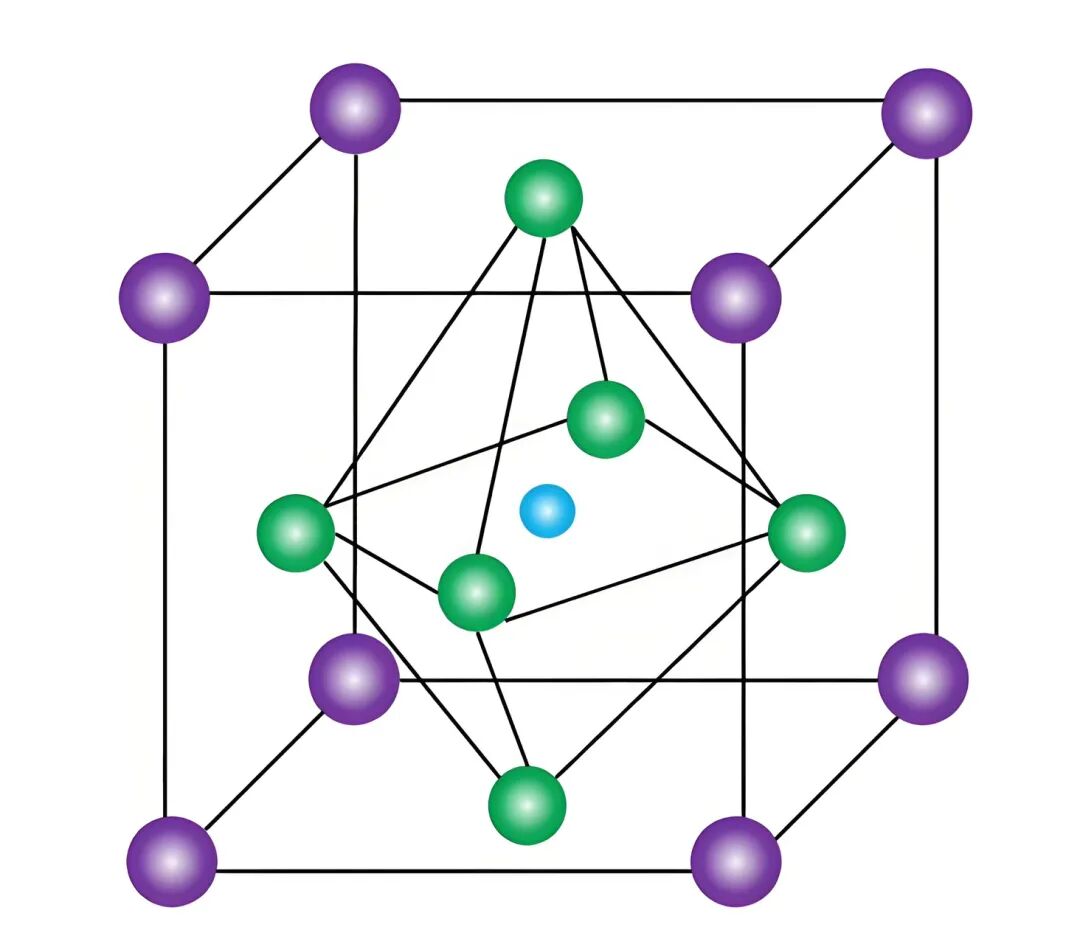
其中8顶为Ca(紫球),6面为 O(绿球),这14个微粒共同构成“混合面心立方”。一般面心立方有8个正四面体空隙和4个正八面体空隙,但此处的面心立方中只有体心那个正八面体空隙由6个清一色氧原子构成,其余11个空隙都“不正”,Ti(蓝球)嵌入的就是这个“纯正”空隙。Ti的配位数为自然为6。
顶点Ca在本晶胞中被3个面心O配位,配位数为1.5。顶点由8个晶胞共用,1.5×8=12,即Ca的配位数为12。反之,面心的O被4个顶点Ca配位,同时被2个体心Ti配位,总配位数为6。
金红石
二氧化钛(TiO2)也是金属钛的重要来源。自然界的常见存在形式是红色的金红石,其晶体晶胞如图所示。蓝球为O,红球为Ti。
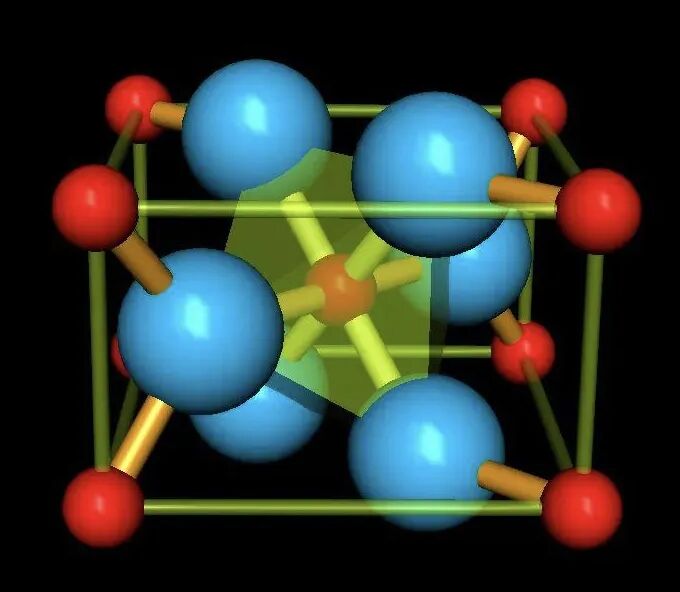
该晶胞属四方晶系,a=b≠c(上下两个面为正四边形),α=β=γ=90º(a=b=c为立方,a≠b≠c称正交)。
晶胞中Ti4+8顶1内,实含2个,O2-4面2内,实含4个,该晶胞的化学式为Ti2O4。
从上往下看,O分三层,一层与三层投影重叠(分别位于面对角线的1/4和3/4处),二层交错(两个O在晶胞体内,垂直投影在一、三层面对角线的1/4和3/4处),可见O呈类似AB密堆积,就是相当于构成六方密堆积。体心的Ti嵌入的是6个O构成的正八面体空隙,可见晶胞顶点上的8个Ti也都居于O构成的正八面体空隙。
依最密堆积(球体接触)计,晶胞上下两面的面对角线长4rO+2rTi,边长为√2(2rO+rTi)。晶胞高相当于密堆六方晶胞之高,c=4√6rO/3。一般离子晶体中阴离子粒径明显大于阳离子,查O2-半径约为140pm,Ti4+半径约为68pm,1:0.4,仍可计得a=b>c。晶胞外形像一块有点扁的方砖。
Ti的配位数为6,O的配位数为3(看晶胞二层的一个O被2顶1心三个Ti等距离配位)。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
一、为什么“摩擦”能加快结晶? 你可以把溶液里的溶质分子想...
一、物质的聚集状态的存在形式 1.通常物质有三态:固态、液...
物质熔点越高,沸点一定也越高吗? 答:不一定。熔点强调的是...
在常见元素中,硼注定是那特别的一个——价层电子只有3个,却...
...
...