
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
确定有机物分子组成是有规律可寻的,下面介绍三种在求解中有重要应用的知识和方法,供同学们在复习时参考。
一、不饱和度
所谓不饱和度是指分子中有多少个双键、叁键和环状结构。计算方法很简单,一般C、H、O、N、X(卤素)的化合物,把N当作CH,X当作H,O略去,这样分子式就变成了烃类的分子式。这个分子式跟烷烃分子式比较,每少2个H原子即称为一个不饱和度。对于分子式为CaHb的烃,其不饱和度Ω=![]() 。一个不饱和度,可能是一个双键,包括C=C、C=O、C=N等等,也可能是一环状结构。两个不饱和度可能是一个叁键,包括C≡C、C≡N,也可能是两个双键或两个环状结构,或者一个双键和一个环状结构,不饱和度更大的化合物也可照此类推,例如苯环就有4个不饱和度。根据不饱和度可以由结构式求分子式,也可以由分子式推断结构式。
。一个不饱和度,可能是一个双键,包括C=C、C=O、C=N等等,也可能是一环状结构。两个不饱和度可能是一个叁键,包括C≡C、C≡N,也可能是两个双键或两个环状结构,或者一个双键和一个环状结构,不饱和度更大的化合物也可照此类推,例如苯环就有4个不饱和度。根据不饱和度可以由结构式求分子式,也可以由分子式推断结构式。
例1、有机环状化合物A的结构简式可进一步简写为B式。C式是1990年公开报导的第1000万种新化合物。则化合物C中的碳原子数是_____,分子式是_____。若D是C的同分异构体,但D属于酚类化合物,而且结构式中没有—CH3基团。请写出D可能的结构简式(任意一种,填入上列D方框中)。
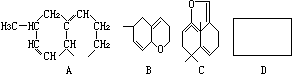
解析:C中的碳原子数为14个,有五个不饱和度,跟具有14个碳原子的烷烃相比少2×5=10个氢原子,所以C的分子式为C14H20O;D属于酚类化合物,结构中必有苯基和酚羟基,苯基有4个不饱和度,所以D的侧链中必有1个不饱和度,它可能是一个双键、或一个环,存在于碳链的末端,这样在结构式中才能没有—CH3基团,答案略。
例2、某烃B分子式是C1398H1278;它由4种基团组成,这四种基团分别是:
已知,该分子结构中没有发现苯环连接苯环,也没有发现炔键连接炔键的情况,并且上述基团在连接时不形成新的环状结构,试求B分子中含有四种基团各几个(请列式求解)。
解析:本题有4个未知数,由①分子各碎片的碳原子数,②氢原子数和③不饱和度数应该分别和分子中总的碳原子数、氢原子数和不饱和度数相等,可以得到三个方程式,但还要找第④个方程式的立式条件。如果将“芳环上的余价应该等于脂肪链上的余价”列成等式,就解决了这个问题。
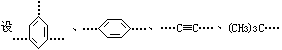 的个数分别为w、x、y、z。则由碳原子数、氢原子数和不饱和度数及芳环上的余价和脂肪链上的余价相等4个条件,得4个方程式:
的个数分别为w、x、y、z。则由碳原子数、氢原子数和不饱和度数及芳环上的余价和脂肪链上的余价相等4个条件,得4个方程式:
6w+6x+2y+4z=1398
3w+4x+9z=1278
4w+4x+2y=![]() =760
=760
3w+2x=2y+z
联立解之得:w=94,x=33,y=126,z=96。
二、新商余法确定分子式
分子式不但可以表现出物质的元素组成,结合不饱和度还可以看出许多有关结构的信息。由分子量确定分子式有许多方法,这里介绍的新商余法确定分子式快速简捷,其方法为①如果是烃类,![]() =a…b,则分子式为CaHb,分子式还可能为其他形式,这时要减一个C加12个H,直到不能再减为止;②如果是烃的衍生物,则将杂原子的式量都刨除,再依上法,不过求出来的是烃基。
=a…b,则分子式为CaHb,分子式还可能为其他形式,这时要减一个C加12个H,直到不能再减为止;②如果是烃的衍生物,则将杂原子的式量都刨除,再依上法,不过求出来的是烃基。
例3、若A是分子量为128的烃,则其分子式只可能是______或________。若A是易升华的片状晶体,则其结构简式为________。
解析:128÷12=10……8,所以分子式为C10H8,也可能是C9H20,又由于A是易升华的片状晶体,所以其结构简式为![]() 。
。
例4、A、B都是芳香族化合物,1molA水解得到1molB和1mol醋酸。A、B的分子量都不超过200,完全燃烧都只生成CO2和H2O,且B分子中碳和氢元素的总的质量分数为65.2%(即质量分数为0.652),溶液具有酸性,不能使FeCl3溶液显色。
(1)A、B分子量之差为_______。
(2)1个B分子中应该有_____氧原子。
(3)A的分子式是______。
(4)B可能的三种结构简式是________。
解析:根据题意,A+H2O→B+C2H4O2,所以MA-MB=60-18=42。B中至少有3个氧原子,如果有3个氧原子,则B的分子量为48÷(1-65.2%)=138,不可能有4个有氧原子,这样A的分子量将超过200,A中有4个氧原子,其式量为138+42=180,其烃基部分的式量为180-4×16=116,116÷12=9……8,故分子式为C9H8O4。不用再减碳加氢,否则不饱和度无法满足条件。其余略。
例5、1999年合成了一种新化合物,本题用X为代号。用现代物理方法测得X的相对分子质量为64;X含碳93.8%,含氢6.2%;X分子中有3种化学环境不同的氢原子和4种化学环境不同的碳原子;X分子中同时存在C—C、C=C和C≡C三种键,并发现其C—C键比寻常的C=C短。
(1)X的分子式是______。
(2)请写出X的可能的结构式。
解析:64÷12=5……4,所以分子式为C5H4,结构为![]() 。
。
三、分子式的等价变形
只含C、H、O的有机物,为便于研究其完全燃烧时,反应物、生成物与所需氧气量的关系,可将其分子式用通式(CxHy)m(H2O)n、(CxOy)m(H2O)N或(CxHy)M(CO2)n表示(m、n、x、y均为正整数),这样再研究有关燃烧的问题时,将会事半功倍。
例6、现有一类只含C、H、O的有机物,它们燃烧时消耗的O2和生成的CO2的体积比为5∶4,在这类化合物中,相对分子量最小的物质的分子式是______;生成的CO2和生成H2O物质的量之比为1∶1,且能发生水解反应的物质的分子式是_______。
解析:在应用前述变形时,可根据耗氧量与生成的CO2量之比选择应用哪一个式子。这类物质燃烧时消耗的O2和生成的CO2的体积比为5∶4,故选择(CxHy)m(H2O)n,依据耗氧量与生成的CO2量之比列式如下:![]() ∶x=5∶4,整理得x∶y=1∶1,所以这类物质的通式为(CH)m(H2O)n,在这类化合物中,相对分子量最小的物质的分子式是(CH)2(H2O)1,即C2H4O。生成的CO2和生成H2O物质的量之比为1∶1,且能发生水解反应的物质的分子式是(CH)4(H2O)2,即C4H8O2。
∶x=5∶4,整理得x∶y=1∶1,所以这类物质的通式为(CH)m(H2O)n,在这类化合物中,相对分子量最小的物质的分子式是(CH)2(H2O)1,即C2H4O。生成的CO2和生成H2O物质的量之比为1∶1,且能发生水解反应的物质的分子式是(CH)4(H2O)2,即C4H8O2。
例7、取3.40g只含羟基、不含其他基团的液态多元醇,置于5.00L氧气中,经点燃,醇完全燃烧。反应后气体体积减少0.56L。将气体经CaO吸收,体积又减少2.80L(所有体积均在标准状况下测定)。
(1)3.40g醇中C、H、O物质的量分别为C:______mol,H:______mol,O:_______mol,该醇中C、H、O的原子数之比为_________。
(2)由以上比值能否确定该醇的分子式_______,其原因是________。
(3)如果将该多元醇的任意一个羟基换成一个卤原子,所得到的卤代烃都只有一种,试写出该饱和多元醇的结构简式。
解析:醇完全燃烧生成CO2:![]() =0.125mol,耗O2:
=0.125mol,耗O2:![]() =0.150mol,二者物质的量之比为0.150∶0.125=6:5,故设其通式为(CxHy)m(H2O)n,
=0.150mol,二者物质的量之比为0.150∶0.125=6:5,故设其通式为(CxHy)m(H2O)n,![]() ∶x=6∶5,x∶y=5∶4,其通式为(C5H4)m(H2O)n,(C5H4)m的质量为0.125÷5×64=1.60g,式中(H2O)n的质量为3.40-1.60=1.80g,所以H的物质的量为0.125÷5×4+1.80÷18×2=0.300mol,O的物质的量为1.80÷18=0.100mol,所以C∶H∶O=0.125∶0.300∶0.100=5∶12∶4。其余答案略。
∶x=6∶5,x∶y=5∶4,其通式为(C5H4)m(H2O)n,(C5H4)m的质量为0.125÷5×64=1.60g,式中(H2O)n的质量为3.40-1.60=1.80g,所以H的物质的量为0.125÷5×4+1.80÷18×2=0.300mol,O的物质的量为1.80÷18=0.100mol,所以C∶H∶O=0.125∶0.300∶0.100=5∶12∶4。其余答案略。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
【题记】如果把有机分子同分异构体的书写比作是拼积木,那么...
一、过滤 1、原理:根据固体的溶解度不同,将不溶性固体从溶...
一、什么是不饱和度 不饱和度又称缺氢指数或者环加双键指数,...
定义:有机物分子中位置等同的氢叫等效氢. 分子中等效氢原子一...
烃分子式的确定方法有很多,常用的有以下几种: 一、根据烃分...
由有机物的分子式可以快速计算出不饱和度。对于一般简单结构...