
|
学习小专题 |
【络合物】含有络离子的一类复杂化合物,例如冰晶石Na3[AlF6]、硫酸四氨合铜(II)[Cu(NH3)4]SO4、氢氧化二氨合银[Ag(NH3)2]OH等。上述络合物的化学式中,用方括号括起的部分叫络离子,是络合物的内界,方括号以外的部分是络合物的外界。络离子是由中心离子(或原子)和配位体以配位键结合而成。常见的中心离子是过渡元素离子如Fe2+、Fe3+、Cu2+、Ag+、Hg2+等;常见的配位体有F-、Cl-、Cn-、SCN-离子和NH3·H2O等分子。它们之间容易形成络离子如[Fe(SCN)]2+、[Ag(NH3)2]+、[Cu(H2O)4]2+等。络合物的内界与外界以离子键结合,络合物溶于水时,完全电离产生络离子:[Ag(NH3)2]OH [Ag(NH3)2]++2OH-
[Ag(NH3)2]++2OH-
络离子比较稳定,在水溶液中部分电离。
[Ag(NH3)2]+ Ag++2NH3
Ag++2NH3
络合物普遍存在。例如人体中的血红素是Fe3+的络合物,植物体内的叶绿素是Mg2+的络合物。络合物广泛应用于工农业生产和科学技术,例如金的提取、电镀、照相技术,离子的鉴定和测定等。络合物,现称为配位化合物,简称配合物。
【分子间作用力】又称范德华(Van der Waals)力。是物质分子间存在着的作用力, 无方向性, 无饱和性。是短程作用力, 其范围约3~5×10-10 米。分子间作用力比化学键的键能要弱得多, 比化学键的键能小一、二个数量级。分子间作用力有取向力、诱导力和色散力三种, 一般以色散力为主。分子间作用力是决定分子型物质的熔点、沸点、气化热、熔化热以及溶解度、表面张力、粘度等物理化学性质的主要因素。
【色散力】分子间作用力的主要成分。色散力普遍存在于各种分子之间。由于分子中电子不断运动和原子核的不断振动,经常发生电子云和原子核之间的瞬时相对位移, 因而产生了瞬时偶极。瞬时偶极虽然存在的时间极短, 但总是不断地出现。这种由瞬时偶极产生的分子间作用力叫色散力。色散力的大小和分子的变形性、电离势以及分子间的距离有关。
【取向力】分子间作用力的一种。存在于极性分子和极性分子之间。当两个极性分子相互接近时,一个分子带负电的一端要和另一个分子带正电的一端接近, 使极性分子有按一定方向排列的趋势。这种由极性分子的取向而产生的分子间作用力叫取向力。取向力的本质是静电引力,取向力的大小和分子的偶极矩(见偶极矩)的大小、温度及分子间的距离有关。
【诱导力】分子间作用力的一种。存在于极性分子与非极性分子之间以及极性分子和极性分子之间;离子和分子以及离子和离子之间。当极性分子和非极性分子接近时, 极性分子的偶极使非极性分子极化而产生诱导偶极, 这种由于诱导偶极而产生的作用力叫诱导力。极性分子之间, 离子和分子以及离子和离子之间也会产生诱导力。诱导力的大小和分子的偶极矩、变形性及分子间距离有关。
【说明 】
1.分子间作用力首先是由荷兰物理学家范德华提出的,因此又叫范德华力。由于这种力的存在,常温下是气态的物质,在降温和加压时能够凝聚成液态,再能凝结成固态的分子晶体。在发生物态变化时分子的组成不变,只是分子间距离缩短(或伸长),分子的运动逐步由无序向有序(或者相反)过渡。
2.分子间作用力约比化学键的作用力小1一2个数量级。分子间作用力约为每摩尔几个到几十个千焦,作用力范围约为300 一500 pm。
3.分子间作用力来源于分子间的取向力、诱导力和色散力。取向力只存在于极性分子间,是极性分子间靠具有电性的永久偶极间的相互作用。诱导力存在于极性分子间和极性分子与非极性分子间。非极性分子受极性分子偶极电场的影响,能使正、负电荷中心发生位移,产生诱导偶极。诱导偶极和极性分子永久偶极间的作用力就是诱导力,又叫变形极化作用力。色散力又叫瞬时极化作用力,普遍存在于各种分子之间,因为非极性分子也会由于电子运动和原子核振动而发生瞬时相对位移而形成瞬时偶极,于是瞬时偶极间发生相互作用。
分子中三种作用力哪种占优势,取决于相互作用分子的极性和变形性。例如,在卤化氢(HF除外)分子中,HCl分子的极性最大,它的诱导力和取向力也最大;HI的变形性最大,它的色散力最大。极性小的分子间主要存在色散力,取向力和诱导力占的比重极小;极性大的分子之间,取向力和诱导力所占比重明显增大。
4.分子间作用力是决定物质物理性质(如熔点、熔化热、沸点、气化热、溶解度、表面张力和粘度等)的主要因素。因此,可以根据相似物质的分子间作用力大小来推断这些物质物理性质的递变规律。
【定义】氢键是特殊的分子间或分子内的作用。它是由极性很强的A一H键上的氢原子跟另F个键(可存在于同一种分子或另一种分子中)上电负性很强、原子半径较小的B原子(如F、O、N 等)的孤对电子之间相互吸引而成的一种键(A一H…B)。
【说明】
1.当电负性很大的F、O、N原子和H形成极性很强的F一H、0一H、N一H键时,它们中共用电子对基本上偏向于这些电负性大的原子一边,使H原子几乎成为“裸露”的氢核。氢核的半径很小,带δ+的氢核对另外的F、O、N原子有强烈的静电作用,这就形成氢键。
2.氢键可以用A一H…B表示。A和B可以是同种原子,也可以是不同种原子,但都是电负性较大、半径极小的非金属原子。表示式中的实线表示共价键,虚线表示氢键。H和B两原子中心的距离就是氢键的键长。氢键的键能一般小于40kJ/mol,共价键的键能小得多,比较接近分子间作用能。因此氢键不属于化学键,而属于一般分子间力范畴。
3-在A一H…B中,为了使A和B原子中电子云之间斥力最小,所成氢键较强,体系较稳定,A和B应尽量距离远一些,故A一H…B必须在同一直线上。这表明氢键有方向性。另外,H 的原子半径比A和B小得多。当形成A一H…B后,如再有另外的A或B靠近它们时,这个原子的电子云会受原先氢键中A、B 中电子云的排斥,因此一个H原子不能再形成第二个氢键。这表明氢键具有饱和性。
4.氢键的强弱跟A、B元素的电负性和原子半径大小有关。半径越小、电负性越大,形成的氢键越强。碳原子的电负性较小,一般不易形成氢键。氯原子的电负性虽大,但原子半径较大,因而形成的氢键也很弱。
5.用氢键的形成可以解释水、氢氟酸、氨等沸点的反常现象,解释醇、甲酸、乙酸沸点较高以及氨、低级醇易溶于水的原因。因此,氢键的形成会使化合物的性质(如熔点、沸点、溶解度)发生很大变化。由于一般的糖、蛋白质、脂肪中都含有氢键,因此氢键在生物化学中有特别重要的意义。
6. 当在苯酚的邻位军有一CHO、一COOH、一N02等基团时,酚羟基中的氢原子可能跟这些基团中的氧原子形成分子内氢键,生成螯合环。如硝酸分子内的氢键:
氨分子中的氮原子上有一对孤对电子,氢离子的1s是空轨道。NH3与H+ 反应时,N原子上的孤对电子进入H+ 的1s轨道,成为N与H两原子的共用电子对,形成了配位键。其中的4个共价键是完全等同的,它们的键长、键能和键角均相等,构成正四面体的空间结构。又如水合氢离子也是以配位键形成的。
水分子中的氧原子上有二对孤对电子,其中一对进入H+ 的1s空转道,形成了配位键。形成配位键必须具备两个条件:①一个原子要有能接受孤对电子的空轨道;②另一个原子要具有能提供的孤对电子。
3.在配合物形成过程中,主要是配位键在发生作用。习惯上,把配体向中心离子提供孤对电子的叫做正常配位键,由中心离子或原子向配位体提供电子的叫反配位键。例如,在羰基配合物中有反配位Π键。
【定义】由分子中正、负电荷重心是否重合,会引起分子有、无极性的现象。
【说明】
1. 当整个分子中正、负电荷重心不相重合时,就形成两个“极”。这正、负两极叫做偶极。这样的分子是有极性的。如果正、负电荷重心相重合,这样的分子没有极性。
2.分子极性的强弱可用分子偶极矩μ来度量。分子的偶极矩越大,分子的极性越大。
3.由同种原子组成的双原子分子没有极性,μ=0。
由典型的金属和典型的非金属组成的气态离子型分子,正、负电荷的重心的分离程度就足够大,这是极性分子的一种极端情况。
由不同原子组成的共价型双原子分子都有极性,μ≠0。分子极性的大小随两元素电负性差的减小而减小。例如,从HF到HI,μ不断减小。
在多原子分子中,如果各个键的偶极矩矢量和为0,分子没有极性,例如CO2是直线形分子(O=C=O),分子中两个C=O极性键对称地分布在碳原子的两边,两个键的极性互相抵消,CO2是非极性分子。三氟化硼分子为平面正三角形,甲烷分子是正四面体结构,这些分子由于结构对称,键的极性互相抵消,正、负电荷重心重合,均为非极性分子。
又如水分子是V形分子,两个H—O极性键偏向分子的一端,整个分子正、负电荷重心不重合,是极性分子。氨分子呈三角锥形,也是极性分子。
4. 由于分子有无极性和极性大小都会影响分子间的作用力,因而分子的极性也是决定物质熔点、沸点、溶解性以及分子的电、磁性质的重要因素。
分子的极性会影响物质的性质如溶解性,极性分子易溶于极性溶剂,非极性分子易溶于非极性有机溶剂。例如,NH3、HCl极易溶于水,难溶于有机溶剂。而Br2、I2难溶于水,易溶于CCl4,苯、汽油等。根据物质在不同溶剂中具有不同的溶解性,可用液-液萃取分离的方法分离提纯物质。
【偶极矩】是衡量分子极性大小的物理量。物理学中,把大小相等、符号相反、彼此相距为d的两个电荷(+q和—q)组成的体系称为偶极子,其电量与距离之积就是偶极矩(μ)。公式为:μ=qd,偶极矩是矢量,其方向系沿两电荷连线由正到负。极性分子就是偶极子,对分子中正负电荷,可以设想它们分别集中于一点,叫正电荷中心和负电荷中心。极性分子的偶极矩等于正负电荷中心的距离乘以正电中心(或负电中心)的电量,其方向由正到负。
【定义】正、负电荷中心间的距离r和电荷中心所带电量q的乘积,叫做偶极矩μ=r×q,它是一个矢量,方向规定为从正电荷中心指向负电荷中心。偶极矩的单位是D(德拜)。
【说明】
1.根据讨论的对象不同,偶极矩可以指键偶极矩,也可以是分子偶极矩。分子偶极矩可由键偶极矩经矢量加法后得到。
2.实验测得的偶极矩可以用来判断分子的空间构型。例如,同属于AB2型分子,C02的μ=0,可以判断它是直线型的;H2S 的μ≠0,可判断它是折线型的。
3.可以用偶极矩表示极性大小。键偶极矩越大,表示键的极性越大;分子的偶极矩越大,表示分子的极性越大。
4.一些常见气态分子的偶极矩μ(D)
 |
| 偶极矩 |
【键的极性】 两个原子形成共价键时,由于原子吸引电子的能力不同,共用电子对偏向原子的一方,吸引电子能力强的原子带部分负电荷,吸引电子能力弱的原子带部分正电荷,共价键有了极性,称为极性共价键,简称极性键。共价键的极性与两成键原子吸引电子的能力(即电负性)的差值有关。同种元素的原子成键时,两原子吸引电子的能力相同,电子对无偏向,形成非极性共价键;不同种元素的原子成键时,共用电子对偏向吸引电子能力强的原子,形成极性共价键。两原子吸引电子能力的差值越大,键的极性越强,当这种差值大到一定程度时,电子从一个原子转移到另一个原子,共价键转变成离子键。
H-H H-I H-Br H—Cl H-F Na+ F-
| | C-C单健 | C=C双键 | C≡C叁键 |
|---|---|---|---|
| 键长(10-10 米) | 1.54 | 1.34 | 1.20 |
| | F—F | Cl-Cl | Br—Br | I—I |
|---|---|---|---|---|
| 键长(10-10 米) | 1.418 | 1.988 | 2.284 | 2.666 |
| | H—F | H-Cl | H—Br | H-I |
| 键长(10-10 米) | 0.918 | 1.274 | 1.408 | 1.608 |
| 键 型 | C-C | C=C | C☰C | N-N | N=N | N☰N |
|---|---|---|---|---|---|---|
| 键长(pm) | 154 | 134 | 120 | 145 | 125 | 110 |
| | C-C单健 | C=C双键 | C≡C叁键 |
|---|---|---|---|
| 键长(10-10 米) | 1.54 | 1.34 | 1.20 |
【等电子体】具有相同电子数的分子或离子称等电子体。例如,都含有14个电子的CO和N2两种分子,就是等电子体。在一般情况下,等电子体在分子轨道中的电子排布和成键情况是相似的,这一规律称作等电子原理。由于等电子体具有相似的结构,所以在性质上也有许多相似之处。如:
| CO |
N2 |
|
| 分子量 | 28 |
28 |
| 熔点(K) | 73 |
63 |
| 沸点(K) | 83 |
77 |
| 液体密度(g·cm-3) | 0.793 |
0.796 |
另外,如NO3-和CO32-也是等电子体或称等电子离子,它们的几何构型都是平面三角形;PO43-、SO42-、ClO4-三种等电子离子的几何构型都是正四面体。
【定义】由同种分子结合成较复杂的分子,但又不引起化学性质改变,这种现象叫做分子缔合。
【说明】
1.HF、NH3、H2O等分子容易发生分子缔合,主要原因是形成了氢键。形成的分子叫缔合分子。分子发生缔合时放热。
2. 水分子发生缔合,xH2O (H2O)x十热量。在固态时,大量水分子以氢键互相连接成巨型缔合分子。其中每个氧原子跟两个氢原子紧靠,形成O-H键(键长为101 pm,键角为109°28',比原来104.5°稍稍扩张),而跟另外两个氢原子相距很远,形成键长276 pm 的氢键。这个结构向空间无限周期性地延伸,就形成冰晶体。冰的结构比较疏松,出现密度比水小的特殊性质。
(H2O)x十热量。在固态时,大量水分子以氢键互相连接成巨型缔合分子。其中每个氧原子跟两个氢原子紧靠,形成O-H键(键长为101 pm,键角为109°28',比原来104.5°稍稍扩张),而跟另外两个氢原子相距很远,形成键长276 pm 的氢键。这个结构向空间无限周期性地延伸,就形成冰晶体。冰的结构比较疏松,出现密度比水小的特殊性质。
当冰熔化成液态水时,部分氢键遭到破坏,部分缔合作用消除,但仍有许多运动自由的、以氢键结合的小集团(x=2,3,4,…),不断地变动、改组,且可堆积得较为紧密。因此冰熔化时体积反而缩小。
在气态时,缔合作用完全消失,水就以单个分子存在。
3.分子缔合作用除了形成氢键的原因外,还可以通过极性分子中偶极的相互作用,以及通过形成配位键(如AlCl3二聚体)而缔合。
【分子轨道理论】又称分子轨道法(Molecular OrbitalTheory)或MO法,1932年由美国化学家密立根(R.S.Mul-liken)及德国物理学家洪特(F.Hund)提出。是现代共价键理论之一。它的要点是:从分子的整体性来讨论分子的结构,认为原子形成分子后,电子不再属于个别的原子轨道,而是属于整个分子的分子轨道,分子轨道是多中心的;分子轨道由原子轨道组合而成,形成分子轨道时遵从能量近似原则、对称性一致(匹配)原则、最大重叠原则,即通常说的“成键三原则”;在分子中电子填充分子轨道的原则也服从能量最低原理、泡利不相容原理和洪特规则。
【分子轨道】分子中描述单电子运动状态的波函数即为分子轨道,分子轨道由原子轨道线性组合而成,原子轨道形成分子轨道时遵从“成键三原则”。
【成键分子轨道】能量相近的原子轨道组合形成的分子轨道中,比原子轨道的能量有所降低的叫做成键分子轨道。在成键分子轨道中,两核间电子出现的几率增大,其能量比原子轨道中能量较低的还低,因此有利于化学键的形成。
【反键分子轨道】能量相近的原子轨道组合形成的分子轨道中,比原子轨道的能量有所升高的称反键分子轨道。在反键分子轨道中,两核间电子出现的几率减小,甚至为零,其能量比原子轨道中能量较高的还高,因此不利于化学键的形成。反键轨道通常以“*”号标记。
【成键三原则】指原子轨道组合形成分子轨道时所遵从的能量近似原则、对称性匹配原则和轨道最大重叠原则。
【现代价键理论】又称电子配对理论或电子配对法,简称VB法(Valence Bond Theory)。基本要点如下:
(1)原子带有未成对且自旋相反的电子相互接近时,核间电子云密度较大,可形成稳定的化学键。
(2)共价键有饱和性,一个原子有几个未成对电子,就能和几个自旋相反的电子配对成键,未成对电子都配对成键就达到饱和。
(3)共价键有方向性,即共价键尽可能沿着原子轨道最大重叠的方向形成,这也叫做“最大重叠”原理。轨道重叠越多,电子在两核间出现的几率就越大,形成的共价键就越稳定。
现代价键理论模型直观,易于人们接受,但解释某些分子形成(如H2+,O2)等遇到了困难。这些问题由于分子轨道理论的建立才得以解决。
【离子的极化作用】电荷相反的离子相互接近时就有可能发生极化,即它们在相反电荷的电场的影响下电子云发生变形。离子使异号离子极化而变形的作用称为该离子的极化作用。
离子极化作用的大小跟离子所带电荷的多少、离子半径大小及离子构型有关。一般离子所带电荷数越大,半径越小,外层电子的屏蔽作用越小,离子的极化作用就越大。通常阳离子的极化作用较强,因此在多数情况下应考虑阳离子对阴离子的极化作用。有的阴离子对阳离子也有显著的极化作用,而阳离子被极化后又对阴离子产生更强的极化作用。这样反复作用叫做离子的相互极化作用或附加极化作用。
离子的极化对化合物的键型、溶解度、熔点、颜色及化学稳定性都有一定的影响。
【定义】在配合物中,跟配合物形成体(中心原子或离子)直接结合的配位原子总数,叫配位数。
【说明】
1. 直接结合的配位原子总数,就是各配位体配位原子数的总和。对单齿配体(即一个配体只有一个被结合的配位原子)来说, 配位数就是配体数。如果是双齿或多齿配体,一个配体上被结合的配位原子数不止一个,则配位数就不是配体数,但仍然是直接结合的配位原子数目。
2. 配位数跟中心原子、配体的大小和它们的氧化态有关。 一般说来,随中心原子(或离子)的半径增大,氧化态升高而配位数增大。同一种中心原子(或离子)在不同配合物中的配位数不是固定不变的,例如[CoCl4]2-和[Co(NH3)6]2+ ; [Ni(CN)4]2- 和[Ni(CN)5]3-
3. 除了中心原子和配位体的结构因素外,配合物形成的条件,如温度、浓度等对配位数也有影响。一般说,低温、高浓度有利于形成高配位数配离子。此外,配位数还跟化合物的物理状态、有没有聚合作用等因素有关。例如,固态的MoC15是双聚分子,Mo的配位数不是5而是6。
4. 目前发现的配合物中,配位数的范围从2〜12都有。其中以4、6为最多、最普遍;配位数为8的正在多起来,2、3、5、7较少见,9~12的更少见。五配位的在过渡金属为中心原子的配合物中也经常遇到,它可以形成双三角锥或四方锥形两种结构。
5. 在讨论各种类型晶体结构时,也常借用配位数这个名词, 系指一个原子(或离子)周围连接的其他原子(或异号离子)的数目。
【定义】原子在成键时受到其他原子的作用,原有一些能量较近的原子轨道重新组合成新的原子轨道,使轨道发挥更高的成键效能,这叫做轨道杂化。形成的新原子轨道叫做杂化轨道。
【说明】
1. 轨道杂化概念,是由美国化学家鲍林在1931年首先提出的,经过不断深化和完善,现已成为当今化学键理论的重要内容之一。 '
2. 杂化轨道的成键能力比原轨道的成键能力大大提高。因此由杂化轨道成键时给体系带来的稳定能,远远超过杂化时需要能量。
3. 由n个原子轨道参加杂化而形成n个能量相等、成分和形状完全相同,仅空间方位不同的杂化轨道,这样的杂化方式叫等性杂化。不同的等性杂化方式会形成不同几何构型的分子结构。例如,1s个轨道,3个p轨道发生sp3杂化,形成4个sp3杂化轨道,这样形成的分子呈正四面体构型。由sp2杂化形成的分子呈平面三角形,由sp杂化形成的分子呈线型。过渡元素常有d轨道参与杂化,如由d2sp3杂化形成的正八面体分子,由d2sp2杂化形成的平面正方形分子,由dsp3杂化形成的三角双锥分子。
4. 当原有能量较近的原子轨道没有全部参加杂化时,如 sp2、sp杂化,就会有多余的p轨道留下来进行侧面重叠,形成Π型轨道或多中心离域大Π轨道。
5.如果原有的价电子层上有富余的价电子(如N、0、C1 等),则常形成不完全等同的杂化轨道。这些轨道除了空间方位不同外,能量、成分、形状都不完全相同。其中有的用以成键,有的被自已的孤对电子占用,如H2O、NH3分子等。H2O分子中氧原子 采取不等性作sp3杂化,形成四个不完全等同的杂化轨道,其中两两 等价,分别和两个氢原子成键及被氧原子的两对孤对电子占有。 这些被孤对电子占用的杂化轨道,在合适的条件下也能再跟另一 原子的空轨道形成配位键,如H30+、NH4+等。
【定义】在单原子分子或以共价键结含的分子中,分子和分子之间存在的一种比化学键弱的相互作用力,叫做分子作用力。
【说明】
1. 分子间作用力首先是由荷兰物理学家范德华提出的,因此又叫范德华力。由于这种力的存在,常温下是气态的物质,在降温和加压时能够凝聚成液态,再能凝结成固态的分子晶体。在发生物态变化时分子的组成不变,只是分子间距离缩短(或伸长),分子的运动逐步由无序向有序(或者相反)过渡。
2. 分子间作用力约比化学键的作用力小1〜2个数量级。分子间作用力约为每摩尔几个到几十个千焦,作用力范围约为300〜500 pm
3. 分子间作用力来源于分子间的取向力、诱导力和色散力。 取向力只存在于极性分子间,是极性分子间靠具有电性的永久偶 极间的相互作用。诱导力存在于极性分子间和极性分子与非极性分子间。非极性分子受极性分子偶极电场的影响,能使正、负电荷中心发生位移,产生诱导偶极。诱导偶极和极性分子永久偶极间的作用力就是诱导力,又叫变形极化作用力。色散力又叫瞬时极化作用力,普遍存在于各种分子之间,因为非极性分子也会由于电 子运动和原子核振动而发生瞬时相对位移而形成瞬时偶极,于是瞬时偶极间发生相互作用。
分子中三种作用力哪种占优势,取决于相互作用分子的极性和变形性。例如,在卤化氢(HF除外)分子中,HC1分子的极性最大,它的诱导力和取向力也最大;HI的变形性最大,它的色散力最大。极性小的分子间主要存在色散力,取向力和诱导力占的比重极小;极性大的分子之间,取向力和诱导力所占比重明显增大。
4. 分子间作用力是决定物质物理性质(如熔点、熔化热、沸 点、气化热、溶解度、表面张力和粘度等)的主要因素。因此,可以根据相似物质的分子间作用力大小来推断这些物质物理性质的递变规律。
【概述】两个原子轨道沿键轴方向重叠而形成的一种以两个原子核之间的直线为对称轴的共价键叫σ键。构成σ键的电子叫σ电子。σ键是原子轨道沿轴向重叠的, 具有较大的重叠程度, 因而比较稳定。σ键可以自由旋转, 而不影响电子云的分布。
【定义】由两个相同或不相同的原子轨道沿轨道对称轴方向相互重叠而形成的共价键,叫做σ键。下面是它的形成示意图。
 |
| σ键 |
【说明】
1. σ键是原子轨道沿轴方向重叠而形成的,具有较大的重叠程度,因此σ键比较稳定。σ键是能围绕对称轴旋转,而不影响键的强度以及键跟键之间的角度(键角)。
2. 根据分子轨道理论,两个原子轨道充分接近后,能通过原子轨道的线性组合,形成两个分子轨道。其中,能量低于原来原子轨道的分子轨道叫成键轨道, 能量高于原来原子轨道的分子轨道叫反键轨道。以核间轴为对称轴的成键轨道叫σ轨道, 相应的键叫σ键。以核间轴为对称轴的反键轨道叫σ* 轨道, 相应的键叫σ* 键。分子在基态时,构成化学键的电子通常处在成键轨道中,而让反键轨道空着。
【概述】成键原子的未杂化的p轨道, 通过平行侧向重叠所形成的共价键叫π键。两个p轨道侧向重叠, 其重叠程度比轴向重叠的σ键小, 稳定性不如σ键, 两个p轨道在平行时才能较大地重叠, 当形成π键的两个原子以核间轴为轴相对旋转时, 会使p轨道重叠程度减小, 导致π键的破坏, π键电子云密集在核间轴平面的上面和下面两部分, 受两核的吸引力较弱, 有较大的流动性。
【定义】成键原子的未杂化p轨道,通过平行、侧面重叠而形成的共价键,叫做π键。它的示意图如下。
【说明】
1. π键是由两个p轨道从侧面重叠而形成的,重叠程度比σ键小,所以π键不如σ键稳定。当形成π键的两个原子以核间轴为轴作相对旋转时,会减少p轨道的重叠程度,最后导致π键的断裂。
2. 根据分子轨道理论,两个原子的p轨道线性组合能形成两个分子轨道。能量低于原来原子轨道的成键轨道π和能量高于原来原子轨道的反键轨道π* ,相应的键分别叫π键和π* 键。分子在基态时,两个P电子(π电子)处于成键轨道中,而让反键轨道空着。
 |
| π键 |
【定义】电荷相反的离子相互接近时就有可能发生极化,即它们在相反电荷的电场的影响下电子云发生变形。离子使异号离子极化而变形的作用称为该离子的极化作用。
【说明】
1.离子极化作用的大小跟离子所带电荷的多少、离子半径大小及离子构型有关。一般离子所带电荷数越大,半径越小,外层电子的屏蔽作用越小,离子的极化作用就越大。通常阳离子的极化作用较强,因此在多数情况下应考虑阳离子对阴离子的极化作用。有的阴离子对阳离子也有显著的极化作用,而阳离子被极化后又对阴离子产生更强的极化作用。这样反复作用叫做离子的相互极化作用或附加极化作用。
2.离子的极化对化合物的键型、溶解度、熔点、颜色及化学稳定性都有一定的影响。
【孤电子对】也称孤对电子。指分子或离子中某原子的最外层未共用的电子对。例如,NH3分子中,N原子有一个孤电子对;H2O分子中,O原子上有两个孤电子对:
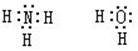
N、O原子都是多电子原子,H原子是等电子原子,因此在NH3分子和H2O分子中都有孤电子对。
【价电子对互斥(VSEPR)理论】该理论最初由西奇威克(Sidgwiek)和鲍威尔(Powell)提出,以后吉林斯比(Gil-lespie)和宁荷姆(Nyholm)发展了这一理论。它的概念非常简单,不需要用原子轨道的概念,就能较好地判断许多共价分子的几何构型。价电子对互斥理论认为在一个共价分子中,中心原子周围电子对排布的几何构型主要决定于中心原子的价电子层中的电子对数,价电子对包括成键的σ电子对和孤电子对。分子的几何构型总是采取彼此间排斥力最小的结构,因为这样能量最低。根据价电子对互斥理论,得出理想的几何构型如下:
| 电子对数 | 几何构型 |
|---|---|
| 2 | 直线型 |
| 3 | 平面三角形 |
| 4 | 四面体 |
| 5 | 三角双锥 |
| 6 | 八面体 |