|
1.
工业制备:
以工业处理钛铁矿为例,分析钛的冶炼原理及条件。
钛铁矿开采后,经粉碎、选矿等处理后得到钛铁矿的精矿砂,以湿法进行冶炼,其目的是将精矿砂经过化学处理转变为可溶性的化合物。湿法冶炼的大致过程如下:
第三步过程是水解:除铁后的硫酸钛、硫酸钛酰溶液经水解(必要时可加入少量晶种)转变为偏钛酸。反应方程式为:
Ti(SO4)2
+ H2O 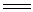 TiOSO4
+ H2SO4 TiOSO4
+ H2SO4
TiOSO4 + H2O
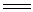 H2TiO3
+ H2SO4 H2TiO3
+ H2SO4
第四步过程是锻烧:将上步水解得到的偏钛酸沉淀经过滤、干燥后进行锻烧,得到二氧化钛。
H2TiO3  TiO2
+ H2O
TiO2
+ H2O
第五步过程是氯化、冶金:由于TiO2不易被还原,常常先将TiO2转变为氯化物。要制成钛锭,还必须在氩气氛中,用极强的还原剂,如金属钠或熔融的金属镁还原TiCl4,制得海绵状钛,再经真空电弧熔融可得钛锭。
TiO2 + 2C +
2Cl2 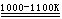 TiCl4 + 2CO TiCl4 + 2CO
|
TiCl4 + 2Mg |

|
Ti + 2MgCl2
|

1.
工业制备:
目前工业上生产二氧化钛的方法主要有两种:即硫酸法和氯化法。
硫酸法是将内含TiO2约50%的钛铁矿和93%的硫酸,以一定的比例加入酸解器中,在压缩空气搅拌下,通蒸气加热至353K,使钛铁矿分解,制得可溶性的硫酸钛酰(TiOSO4)。
FeTiO3 + 2H2SO4 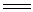 TiOSO4
+ FeSO4 + 2H2O
TiOSO4
+ FeSO4 + 2H2O
产物经浸取,再加铁屑,使杂质沉降除去。清液置于冷冻器中,冷至276~278K。使副产品硫酸亚铁结晶析出。滤液经减压蒸发、浓缩,用蒸气加热水解后,得到白色的偏钛酸。该步骤是生产的关键,为促进反应进行,要求控制在高温、低酸度、低浓度的条件下进行。
TiOSO4 + 2H2O 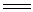 H2TiO3↓+
H2SO4 H2TiO3↓+
H2SO4
将偏钛酸经过滤、水洗、盐处理等后所得的产物,在1073~1123K下煅烧,即可转化成产品二氧化钛。
H2TiO3 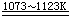 TiO2
+ H2O TiO2
+ H2O
生产过程中的酸性废液,需经废碱处理后,才能排放。

在室温下,α-正钛酸(H4TiO4)通过硫酸钛酰与强碱(NaOH)或氨水反应制得:
TiOSO4 + 2NaOH + H2O 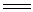 H4TiO4↓+
Na2SO4
H4TiO4↓+
Na2SO4
β-钛酸(H2TiO3)是将可溶性钛盐(如TiOSO4)溶于冷水,然后煮沸水溶液制得:
TiOSO4 + 2H2O  H2TiO3↓+
H2SO4 H2TiO3↓+
H2SO4

1.
工业制法:
工业上以TiCl4为原料,通过氢还原法,铝还原法或钛还原法制备TiCl3。目前工业上以铝还原法最常用。将过量的TiCl4和定量的铝粉加入反应器,使之反应:
3TiCl4 + Al 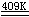 3TiCl3
+ AlCl3 3TiCl3
+ AlCl3
反应后蒸出过量的TiCl4,并使AlCl3升华逸出。为保证产品中TiCl4的残余量低于0.1%,需抽真空。蒸出的TiCl4及AlCl3可循环使用。

1.
工业制备:
工业上主要采用沸腾床氯化法制备TiCl4。将一定粒度的金红石和炭粉装入底部通以氯气的氯化炉中,使之反应:
TiO2 + 2C + 2Cl2 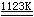 TiCl4
+ 2CO
TiCl4
+ 2CO
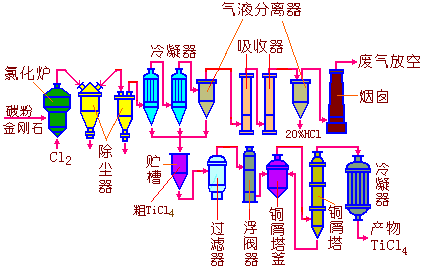
产物TiCl4气体由炉顶逸出,流经两个串联的隔板除尘器,在除尘器中经降温和降速,以除去高沸点杂质。干净的气体经冷凝器冷却至TiCl4的沸点(409K)以下,形成的液态TiCl4经过滤即可得粗制的TiCl4。进一步精制,除去低沸点杂质后,即可得精制TiCl4成品。简易的生产流程图见下图:
|
|
|
图16-2 TiCl4的生产流程图 |

|