|
ïçϵԪËØÖÐÖ»ÓÐîÞÊÇ·ÅÉäÔªËØ£¬½öÔÚÓË¿óÖÐÓкÛÁ¿´æÔÚ£¬ÆäËûïçϵԪËز¢²»Ï¡ÓС£ÎÒ¹úµÄÏ¡ÍÁÔªËز»½ö´¢Á¿Õ¼ÊÀ½çÊ×룬¶øÇÒÏ¡ÍÁ¿óÎïµÄƷλҲ¸ß£¬ÀýÈ磬¶À¾ÓʯÖÐÏ¡ÍÁÑõ»¯ÎïµÄƷλΪ60£¥£¬Á×îÆ¿óÖÐîƵĺ¬Á¿´ï60£¥£¬³ýº¬ÓÐÏ¡ÍÁÔªËØÍ⣬»¹º¬ÓÐNb£¬Ta£¬Ti£¬ThºÍUµÈÔªËØ¡£Ï¡ÍÁ¿óµÄ³É·Ö¼ûϱí
×¢£º1¡¢±íÖÐÊý¾Ý¾ùΪϡÍÁÑõ»¯Îï×ܺ¬Á¿Öи÷³É·ÖËùÕ¼°Ù·Ö±È¡£
×îÓпª²É¼ÛÖµºÍ×îÖØÒªµÄÏ¡ÍÁ¿óÊǶÀ¾ÓʯCePO4¡¤Th3(PO4)4£¬Á×îÆ¿óY(PO4)ºÍ·ú̼îæïç¿ó(Ce,La)FCO3¡£¶À¾ÓʯµÄÖ÷Òª³É·ÖÊÇîʺÍïçϵԪËصÄÁ×ËáÑΣ»Ò²º¬ÓÐÉÙÁ¿µÄÓË¡£Á×îÆ¿óµÄÖ÷Òª³É·ÖÊÇîƺÍïçϵԪËصÄÁ×ËáÑΣ»·ú̼îæïç¿óµÄÖ÷Òª³É·ÖÊÇîæ¡¢ïç¼°ÆäËûïçϵԪËصķú̼ËáÑΡ£
2LnPO4 + 3H2SO4(Ũ)
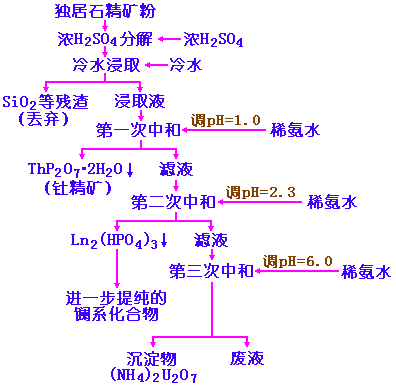
ThSiO4 + 2H2SO4(Ũ) ·´Ó¦Íê±Ïºó£¬²úÎïΪ°µ»ÒÉ«µÄÕ³ÐÔÎïÖÊ£¬ÆäÖк¬ÓÐÏ¡ÍÁÁòËáÑΡ¢îʺÍÓ˵ÄÁòËáÑΡ¢Á×Ëᡢδ·´Ó¦ÍêµÄŨH2SO4ºÍ²»ÈܵIJÐÔüµÈ¡£
È»ºó£¬ÓôóÁ¿ÀäË®½þÈ¡¡£Ê¹ÁòËáÑΡ¢Á×ËáµÈ½øÈëÈÜÒº£¬²¢³ýÈ¥²»ÈܵÄSiO2µÈ²ÐÔü£¬¼´¿ÉµÃµ½Ï¡ÍÁ¡¢îʺÍÓËÁòËáÑεĽþÈ¡Òº¡£
ÔÚÁòËáÑεĽþÈ¡ÒºÖУ¬¼ÓÈëÏ¡°±Ë®£¬½«ÈÜÒºÖкÍÖÁpH£½l£¬²¢¼ÓÈÈÖÁ·Ð£¬´Ëʱ£¬îÊÔò³ÊÄÑÈܵĽ¹Á×ËáÑγÁµíÎö³ö£¬·ÖÀë³öîʵÄÁ×ËáÑΡ£ÂËÒºµÚ¶þ´ÎÓÃÏ¡°±Ë®ÖкÍÖÁpH=2.3£¬Ê¹´ó²¿·ÖïçϵԪËØ£¬ÒÔLn2(HPO4)3ÐÎʽ³Áµí£¬·ÖÀë³öµÄ³Áµí¿É½øÒ»²½ÌáÈ¡´¿µÄïçϵ»¯ºÏÎÂËÒºÓÃÏ¡°±Ë®µÚÈý´ÎÖкÍÖÁpH=6.0£¬ÔòÉú³É(NH4)2U2O7³Áµí£¬³Áµí¿É½øÒ»²½ÌáÈ¡ÓË¡£
Àë×Ó½»»»·¨ÊÇÓÃÀë×Ó½»»»Ê÷Ö¬ÔÚ½»»»ÖùÄÚ·ÖÀë»ìºÏÀë×ӵķ½·¨¡£Ò»°ã°üÀ¨Ê÷Ö¬µÄÎü¸½ºÍÁÜÏ´Á½¸ö¹ý³Ì¡£
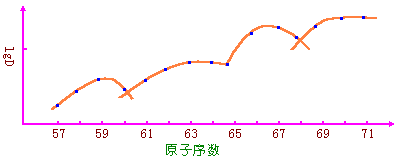
ÓÉÓÚÑôÀë×Ó½»»»Ê÷Ö¬¶ÔÀë×ÓµÄÎü¸½ÄÜÁ¦ÊÇËæÀë×ÓµçºÉµÄÔö¼Ó¶øÔö´ó£¬ËæÀë×Ӱ뾶Ôö´ó¶ø¼õС£¬¹ÊïçϵÀë×ӿɲ»Í¬³Ì¶ÈµØ±»Îü¸½¡£µ«ÓÉÓÚïçϵÀë×ÓLn3+µÄµçºÉÏàͬµ«Àë×Ӱ뾶Ïà²îºÜС£¬±»Îü¸½³Ì¶È²îÒìС£¬¹Êµ¥´¿ÀûÓÃÊ÷Ö¬µÄÎü¸½¹ý³Ì£¬ÎÞ·¨´ïµ½Ê¹»ìºÏïçϵÀë×Ó·ÖÀëµÄÄ¿µÄ¡£
Ln3+(Ê÷Ö¬ÉÏ)+(NH4)3HY(ÈÜÒº)
ÓÉÓÚÀë×Ӱ뾶´ÓLu3+¡ªLa3+µÝÔö£¬ËùÐγɵÄÅäºÏÎïÎȶ¨ÐÔ£ºLuHY×î´ó£¬LaHY×îС£¬Òò´Ë£¬ÔÚÁÜÏ´¹ý³ÌÖУ¬Lu3+Àë×ÓÊ×ÏÈÓëÅäºÏ¼ÁÐγÉÅäºÏÎï¶ø½âÎü£¬¼´Lu3+Ê×Ïȱ»ÁÜÏ´³öÀ´£¬¶øLa3+Àë×Ó×îºóÁÜÏ´³öÀ´¡£ÈôÄܽ«ÁÜÏ´ÒºÖÖÀࡢŨ¶È¡¢Ëá¶È¡¢ÁÜÏ´Ëٶȡ¢½»»»Öù¸ß¶ÈµÈ¿ØÖÆÔÚ×î¼ÑÌõ¼þ£¬Ôò¿É´ÓÁÜÏ´ÒºÖÐÒÀ´ÎÊÕ¼¯µ½´ÓLu3+¡ªLa3+µ¥¸öµÄºÜ´¿µÄïçϵÀë×ÓÈÜÒº¡£È»ºó£¬²ÉÓüӲÝËáµÄ°ì·¨£¬Ê¹Ö®ÒÔïçϵ²ÝËáÑγÁµí´ÓÈÜÒºÖÐÎö³ö£¬¾×ÆÉÕ¼´¿ÉµÃµ½ïçϵÑõ»¯Îï¡£
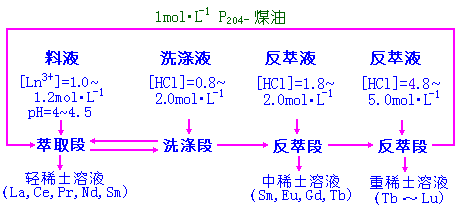
´Ë·¨ÊÇÀûÓÃïçϵÑÎÀàÔÚË®ÏàºÍÓлúÈܼÁ(»òÝÍÈ¡¼Á¼°Ï¡ÊͼÁ)ÖÐÓв»Í¬·ÖÅä±ÈµÄÐÔÖÊ£¬½øÐзÖÀë¡£·ÖÅä±ÈÊÇïçϵÀë×ÓÔÚÓлúÏàÓëË®ÏàÖеÄ×ÜŨ¶È±È£¬D=CÓÐ/CË®£¬·ÖÅä±ÈÔ½´ó£¬ËµÃ÷Ln3+Àë×ÓÔ½Ò×½øÈëÓлúÏà¡£
ÔÚÝÍȡʱ£¬·ÖÅä±È´óÓÚ1µÄÖØÏ¡ÍÁÔªËØÝÍÈ¡½øÈëÓлúÏ࣬·ÖÅä±ÈСÓÚ1µÄÇáÏ¡ÍÁÔªËØÁôÔÚË®Ïà¡£Ln3+Àë×ӵķÖÅä±È£¬ÓëÌåϵËá¶È´óСҲÓйء£ÔÚʵ¼ÊÉú²úÖУ¬¸ù¾ÝË®ÏàËá¶ÈµÄ²»Í¬¿É½«ïçϵ·ÖΪÈý×é¡£
¡¡
½«ïçϵ½ðÊôÓëÑõÖ±½Ó»¯ºÏ(ÔÚ423~453K×ÆÉÕ)£¬»ò½«ïçϵԪËصÄÇâÑõ»¯Îï¡¢²ÝËáÑΡ¢Ì¼ËáÑΡ¢ÏõËáÑλòÁòËáÑÎÔÚ¿ÕÆøÖÐ×ÆÉÕ£¬³ýîæÉú³É»Æ°×É«CeO2¡¢ïèÉú³ÉºÚÉ«Pr6O11(Ï൱ÓÚPr2O3¡¤4PrO2)¡¢ï«Éú³É°µ×ØÉ«µÄTb4O7(Ï൱ÓÚTb2O3¡¤2TbO2)ÒÔÍ⣬ÆäÓà¾ùÉú³ÉÈý¼ÛÑõ»¯ÎïLn2O3¡£ïèºÍï«ÊÇ»ìºÏ¼Û̬µÄÉîÉ«Ñõ»¯ÎËüÃǾùÊÇ·Ç»¯Ñ§¼ÆÁ¿µÄ»¯ºÏÎï¡£½«CeO2£¬Pr6O11ºÍTb4O7ÓÃH2»¹Ô£¬¿ÉµÃµ½+3Ñõ»¯Ì¬µÄÑõ»¯Îï¡£ ¡¡
Ln3+Ó백ˮ»òNaOHÈÜÒº×÷Ó㬼´¿ÉÖƵÃÇâÑõ»¯ÎïLn(OH)3³Áµí¡£
Ln3+ + 3NaOH
Ln3+ + 3NH3¡¤H2O ¡¡
LnCl3¼«Ò×ÈÜÓÚË®£¬ÔÚ¿ÕÆøÖÐÒ׳±½â£¬ÔÚË®ÈÜÒºÖÐ΢ˮ½â¡£´ÓË®ÈÜÒºÖÐÎö³öµÄÂÈ»¯ÎﳣΪÁùË®½á¾§¡£ÈôÒªÖƱ¸ÎÞË®ÂÈ»¯Îï½ÏÂé·³¡£ÓÃÒ»°ã¼ÓÈÈÍÑË®µÄ·½·¨»á²¿·ÖË®½â£¬Éú³ÉÄÑÈÜÓÚË®µÄ¼îʽÑΣº
LnCl3¡¤6H2O Ò»°ã¿ÉÓÃÔÚÂÈ»¯ÇâÆøÁ÷Öн«LnCl3¡¤6H2O¼ÓÈÈÍÑË®µÄ·½·¨ÖƱ¸ÎÞË®ÂÈ»¯ÎÒòÂÈ»¯Çâ¿ÉÒÖÖÆË®½â×÷Óãº
¸ü¼ÑµÄ·½·¨Êǽ«Ln2O3ºÍNH4Cl¹ÌÌå»ìºÏ¹²ÈÈ£¬¼´¿ÉÖƵÃÎÞË®ÂÈ»¯Îï¡£
Ln2O3 + 6NH4Cl(s) ¡¡
Ln(NO3)3Ò×ÈÜÓÚË®£¬ÓÉÈÜÒº½á¾§Îö³öµÄÊÇÁùË®ÏõËáÑΡ£ÏõËáÑÎÊÜÈÈʱ£¬ÏÈ·Ö½âΪ¼îʽÑΣ¬½øÒ»²½ÊÜÈÈÔò·Ö½âΪÑõ»¯Î
2Ln(NO3)3
4LnONO3 ÓÃÕæ¿Õ¼ÓÈÈÍÑË®¸ÉÔï·¨£¬»òÔÚLn(NO3)3¡¤6H2OÖмÓÈëŨÏõËáµÈ·½·¨£¬¾ù¿ÉµÃÎÞË®ÏõËáÑΡ£ ¡¡
³ýÁòËáîæ¡¢ÁòËáïçΪ¾ÅË®ºÏÎïÍ⣬ÆäÓàµÄÁòËáÑξùΪ°ËË®ºÏÎïLn2(SO4)3¡¤8H2O¡£Ë®ºÏÁòËáÑμÓÈÈʱ£¬ËæζȵÄÉý¸ßÒ»°ã¿É·¢ÉúÒÔÏÂÈý²½·´Ó¦£º
Ln2(SO4)3¡¤8H2O
Ln2(SO4)3
(LnO)2SO4 ¡¡
½«²ÝËᾧÌå(H2C2O4¡¤2H2O)»ò±¥ºÍÈÜÒº¼ÓÖÁ¿ÉÈÜÐÔïçϵÑÎÈÜÒºÖУ¬¿É»ñµÃïçϵ²ÝËáÑγÁµí£¬·ÅÖúóת±ä³É½á¾§£º
2Ln3+ + 3H2C2O4 + nH2O
ʽÖнᾧˮһ°ãΪ10£¬Ò²ÓбðÓÚ£¬7£¬9»ò11µÈ¡£ ïçϵˮºÏ²ÝËáÑΣ¬¼ÓÈÈÖÁ313~533Kʱ£¬¿ÉÉú³ÉÎÞË®²ÝËáÑΣº
|