|
1.
工业制备:
大多数的Zn是从硫化矿(主要成分是ZnS,还含有CdS,Ga2S3等)提炼的。冶炼前,常用浮选法先进行富集,获得含ZnS40%~60%的精矿,精矿经氧化焙烧生成ZnO(及CdO等),所得的ZnO可用热还原法或电解法得到金属Zn。
|
2ZnS
+ 3O2 |

|
2ZnO
+ 2SO2↑
|
热还原法是将ZnO与焦炭混合,在鼓风炉中加热至1473K以上,Zn(及Cd等)以蒸气逸出,冷凝即得粗Zn.粗Zn经分馏除去Pb,Cd等杂质可得纯度达99.99%的锌。
电解法是将粗ZnO溶于H2SO4,并加Zn粉置换出不活泼的Cd,Co,Ni,Cu,Ag等杂质,获得精制的ZnSO4溶液,以此ZnSO4溶液为电解液,Pb作阳极,Al为阴极进行电解,在阴极上可得99.95%~99.99%的锌。
|
阳极 4OH-
- 4e 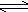 2H2O
+ O2 2H2O
+ O2
|
|
阴极 2Zn2+
+ 4e 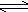 2Zn 2Zn
|
|
总反应 2Zn2+ +
4OH- 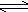 2Zn + 2H2O
+ O2 2Zn + 2H2O
+ O2
|

氧化锌的制备可以由金属锌单质与氧反应或含氧酸盐热分解而制备。
2Zn + O2  2ZnO
2ZnO
2Zn(NO3)2
 2ZnO
+ 4NO2 + O2 2ZnO
+ 4NO2 + O2

工业上生产氯化锌常用金属Zn,ZnO或ZnCO3与盐酸作用,所得溶液经过浓缩、冷却,可得到ZnCl・H2O白色晶体。
ZnO + 2HCl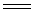 ZnCl2
+ H2O ZnCl2
+ H2O
Zn + 2HCl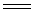 ZnCl2
+ H2 ZnCl2
+ H2
ZnCl・H2O晶体在加热时,不易脱水,而易形成碱式盐:
ZnCl・H2O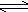 Zn(OH)Cl
+ HCl Zn(OH)Cl
+ HCl
因此,要制备无水ZnCl2,只有将ZnCl2溶液置于氯化氢的气流之下加热脱水。

在锌盐溶液中,加入(NH4)2S,或将Zn(或ZnO)和S一起加热,均可析出白色ZnS沉淀。
ZnCl2 + (NH4)2S 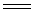 ZnS↓+
2NH4Cl
ZnS↓+
2NH4Cl
2ZnO + 2S 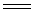 2ZnS + O2 2ZnS + O2

在锌的冶炼过程中,经热还原步骤后(反应在1373K下进行),此时Zn(含有Cd)以蒸气逸出,冷凝得Zn粉(颗粒大小在2~10u之间),因Cd的沸点(1038K)较Zn的低(1180K),故还原得到的Cd在反应条件下先被蒸出,将粗Cd溶于盐酸,然后用Zn置换,可得较纯的Cd。

氧化镉可以由金属单质与氧反应或含氧酸盐,氢氧化物热分解制备.
2Cd + O2  2CdO
2CdO
Cd(OH)2  CdO
+ H2O
CdO
+ H2O

往Cd2+的盐溶液中,分别通入H2S,便生成黄色的CdS沉淀
Cd2+ + H2S 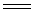 CdS↓
+ 2H+ CdS↓
+ 2H+

1.
工业制备:
辰砂(HgS)是提取汞的主要来源,在空气中将辰砂灼烧至873~973K即可得汞:
|
HgS
+ O2 |

|
Hg
+ SO2
|
也可将辰砂(HgS)与石灰混合焙烧而得汞:
|
4HgS
+ 4CaO |

|
4Hg
+ 3CaS + CaSO4
|
制得的粗汞用稀HNO3洗涤并鼓入空气使比汞活泼的杂质金属均被氧化溶解,生成硝酸盐,不溶的汞进一步真空蒸馏提纯,即得99.99%的纯汞。

汞的氧化物可以由金属汞与氧直接反应,或者向M2+盐溶液加NaOH溶液反应制备。
2Hg + O2 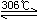 2HgO (温度过高,HgO分解) 2HgO (温度过高,HgO分解)
Hg2+ + 2OH- 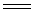 HgO↓+
H2O HgO↓+
H2O

往Hg2+的盐溶液中,分别通入H2S,便生成黑色的HgS沉淀。该沉淀加热至659K时,可转变为稳定的红色HgS变体。
Hg2+
+ H2S 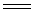 HgS↓+
2H+ HgS↓+
2H+

HgCl2的制备方法如下:
1) 将HgO溶于HCl即可得到HgCl2的白色沉淀:
HgO + 2HCl 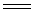 HgCl2
+ H2O
HgCl2
+ H2O
2) 将HgSO4或Hg(NO3)2与NaCl的混合物加热,利用HgCl2易升华的性质,可从产物混合物中得到HgCl2:
HgSO4
+ 2NaCl  HgCl2
+ Na2SO4 HgCl2
+ Na2SO4

1)
在硝酸亚汞溶液中加入盐酸,就生成Hg2Cl2沉淀;
Hg2(NO3)2+
2HCl 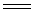 Hg2Cl2↓
+ 2HNO3 Hg2Cl2↓
+ 2HNO3
2) 将氯化汞和汞一起研磨可制得Hg2Cl2:
HgCl2
+ Hg 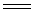 Hg2Cl2 Hg2Cl2
3) 用SO2代替Hg做还原剂,将HgCl2还原成Hg2Cl2:
2HgCl2 + SO2 + 2H2O 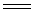 Hg2Cl2↓+
H2SO4 + 2HCl
Hg2Cl2↓+
H2SO4 + 2HCl

用Hg2+盐和适量的碘离子反应,可制得碘化汞沉淀HgI2.
Hg2+ + 2I-  HgI2↓ (橙红色) HgI2↓ (橙红色)

|