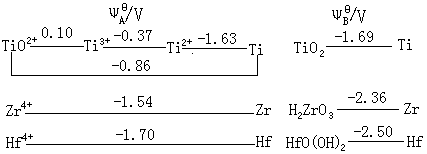|
一:钛族元素基本性质 第ⅣB族即钛族包括钛、锆和铪三种元素,它们元素的基本性质见下表:
二:钛族元素的通性 钛族元素的价电子构型为(n-1)d2ns2,因4个价电子全部参与成键后原子结构(即d 0)比较稳定,所以最稳定氧化态为+4,与族数一致。由于钛元素的原子失去四个电子需要较高的能量,所以它们的M(Ⅳ)化合物主要以共价键结合。 钛还有+3的化合物,但生成+Ⅱ的化合物就很少见。锆和铪生成低氧化态的趋势很小。该族自上而下高氧化态趋于稳定,而低氧化态不稳定。这点与主族元素第ⅣA族中氧化态的变化规律刚好相反。 三:钛族元素标准电势图 钛分族的标准电势图如下:
一:物理性质 钛族金属的外观似钢,纯金属具有良好的可塑性,但有杂质存在时变得脆而硬。锆和铪都是高熔点金属。 二:化学性质 从标准电极电势看,钛、锆和铪是还原性强的金属,但因在金属表面容易形成致密的、钝化的氧化膜,使得钛族金属在通常温度下具有优良的抗腐蚀性,不与酸和碱作用。锆的抗化学腐蚀性优于钛和不锈钢,接近于钽。不过,钛族金属都能溶解在氢氟酸中,生成六氟配合物H2[MF6]。 与常温下的表现相反,钛族金属在高温时能与许多非金属如N、O、B、C等直接化合。 与钪族元素一样,粉末状的钛族金属在高温时能吸附氢气,生成间充化合物MH2。钛族金属的氢化物在空气是稳定的,并不与水反应,这与钪族元素和s区元素的离子型氢化物是显著不同的。 三:锆和铪的相似性* 由于镧系收缩的影响,锆和铪的原子半径和离子半径非常接近,它们的化学性质也很相似,因而二者的分离工作也较困难。目前主要采用离子交换法或萃取法来分离它们。 离子交换法是利用强碱型酚醛树脂R-N(CH3)3+Cl-阴离子树脂,使Zr和Hf转化为配阴离子ZrF62-、HfF62-与阴离子树脂进行吸附交换。由于锆、铪配离子与树脂结合能力不同,用HF和HCl的混合液为淋洗液,可使这两种阴离子先后被淋洗下来,从而达到分离的目的。 |