
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
1、原理:
反应装置内气体体积减小,气压减小,小于外界压差强,在压强差的作用下,吸收液倒流。
2、气体体积减小原因:
(1)反应
①碱性吸收液:酸性气体(酸酐:与对应酸溶液化合价相同),如:CO2、Cl2、H2S、HCl、HBr、N2O5、SO2
②酸性吸收液:碱性气体,如:NH3
③与水反应的气体:Cl2、F2、Br2、NH3、NO2、CO2、SO2
(2)溶解
①极易溶于水的气体:NH3、HCl、HBr
②易溶于水的气体:NO2、SO2
③能溶于水的气体:CO2、Cl2、H2S
④难溶于水的气体:H2、CO、C2H2、C2H4、O2、NO
(3)温度骤冷
3、防倒吸作用
(1)防止液体倒流回热的仪器底部,使仪器炸裂
(2)防止尾气处理装置中的液体倒吸进入发生装置或收集装置中,造成产品的损失。
二、防倒吸装置
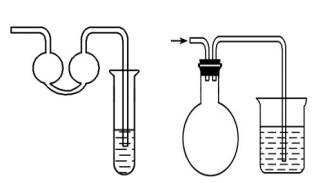
1、倒立漏斗式
①原理:
这种装置可以增大气体与吸收液的接触面积,有利于吸收液对气体的吸收。当易溶性气体被吸收液吸收时,导管内压强减少,吸收液上升到漏斗中,由于漏斗容积较大,导致烧杯中液面下降,使漏斗口脱离液面,漏斗中的吸收液受自身量力的作用又流同城瓶内。从而防止吸收液的倒吸
②仪器装置图:
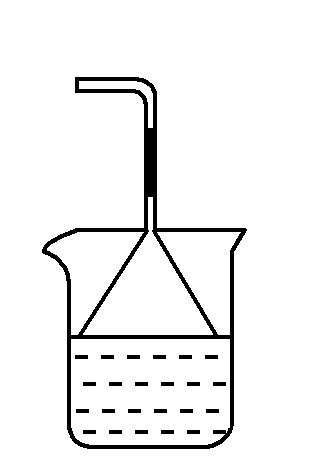
2、肚容式
①原理:
当易溶于吸收液的气体由干燥管末端进入吸收液被吸收后,导气管内压强减小,使吸收液倒吸进入干燥管的吸收液本身质量大于干燥管内外压强差,吸收液受自身重量的作用又流回烧杯内部,从而防止吸收液的倒吸。
②仪器装置图:
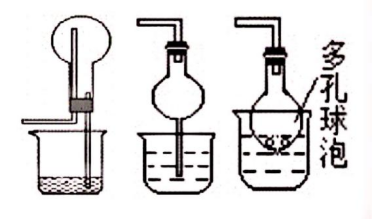
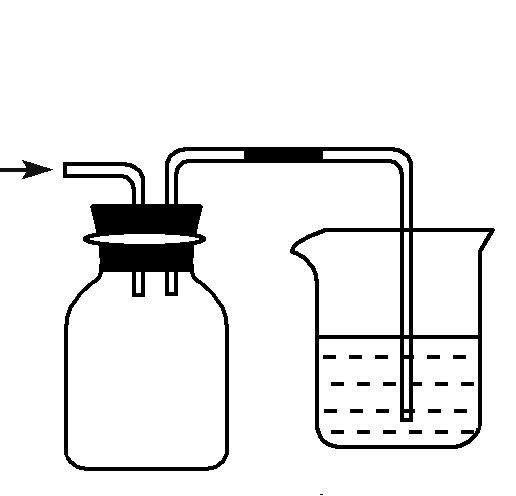
3、隔离式
①原理:
隔离式是在导管末端与液体吸收剂呈隔离状态,这样在气体被吸收的时候不会出现局部压强过小,而起到防倒吸作用。
②仪器装置图:
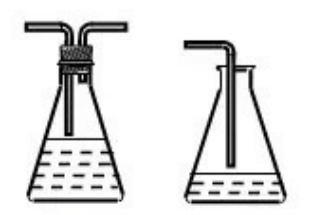
但如上图装置会有缺陷,对于污染性气体,右图可能会使有害气体扩散到空气中,造成二次污染,所以对此方法进行了改进:目前使用较多的是利用气体难溶于某些有机物的性质来进行隔离,比如对于NH3的吸收可以往烧杯中加CCl4和H2O,NH3不溶于CCl4,这样就不会造成局部压强瞬间减小,NH3以气泡的形式进入水中而达到被吸收。有时候会看到苯和H2O这样的组合,这个时候就不能用来处理氨气等易溶于水的气体,因为H2O在下层,这和直接插入水中没有区别,这时要吸收的尾气应该是一些不溶于H2O,但是易溶于有机溶剂的气体,装置如下图所示:
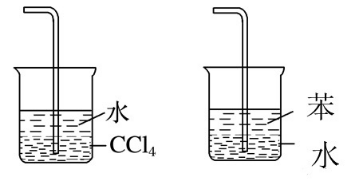
4、蓄液式
①原理:
这种就是采用一个较大容积的容器将可能倒吸来的液体接收,防止进入前端装置。它与肚容式的主要区别是液体不再流回到原容器,而是进入到一个提前装好的装置中,此装置称为安全瓶
②仪器装置图:
三、高考实例
1、倒立漏斗式
【例】(2022・安徽芜湖・三模)硫代硫酸钠(Na2S2O3)可用作分析试剂及还原剂,受热、遇酸易分解。某学习小组用如图装置模拟古法制硫酸,同时利用生成的SO2气体制备硫代硫酸钠。
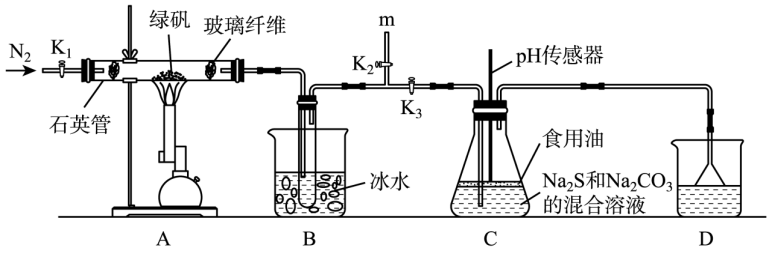
此实验中装置D的作用与目的为吸收残余的SO2,防止倒吸。
此实验防止倒吸的原因为:D为二氧化硫的尾气吸收装置,则D中的溶液应为碱性溶液或水,则二氧化硫会与D中的溶液反应,气体体积减少,会使D中的液体倒流回C中与C中制取硫代硫酸钠的反应物发生反应,使硫代硫酸钠的产率降低。
2、肚容式
【例1】(2022・湖南卷)某实验小组以BaS溶液为原料制备BaCl2・2H2O,并用重量法测定产品中BaCl2・2H2O的含量。设计了如下实验方案:
可选用试剂:NaCl晶体、BaS溶液、浓H2SO4、稀H2SO4、CuSO4溶液、蒸馏水
步骤1.BaCl2・2H2O的制备
按如图所示装置进行实验,得到BaCl2溶液,经一系列步骤获得BaCl2・2H2O产品。
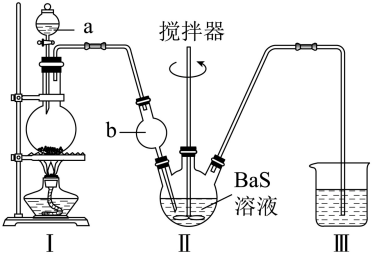
Ⅰ中b仪器的作用是防倒吸。
此实验防倒吸的原因是:装置I为浓硫酸和氯化钠共热制取HCl气体的装置,在浓硫酸过量并微热时,浓硫酸与氯化钠反应生成硫酸氢钠和氯化氢,氯化氢极易溶于水,使II中的硫化钡溶液倒流回热的烧瓶底部,发生炸裂。
【例2】(2022・河南郑州・三模)某同学查阅资料得知,在无水三氯化铝的催化作用下,利用乙醇制备乙烯的反应温度为120℃。反应装置如下图所示:
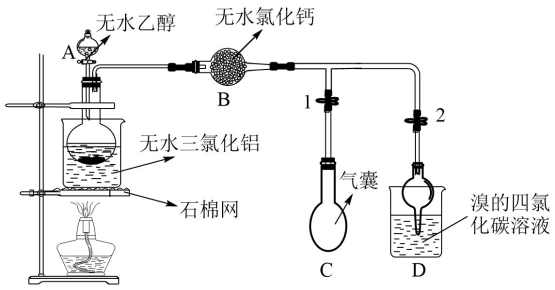
此实验装置D中球星干燥管的作用为防倒吸
此实验需要防倒吸的原因:实验中多余的乙烯与D中的溴的四氯化碳溶液发生加成反应,体积减少,会引发倒吸,会使溴的四氯化碳溶液倒吸进入集满乙烯的C中,与收集到的乙烯反应,造成产品的损失。
3、隔离式
【例】(2021・临沂市兰山区高三开学考试)为探究乙酸乙酯的实验室制备方法,某实验小组设计主要步骤如下:
①在大试管a中配制反应混合液;②按图甲所示连接装置(装置气密性良好),用小火均匀加热大试管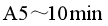 ;③待试管B(内装滴有酚酞的饱和碳酸钠溶液)收集到一定量产物后停止加热,撤去导管并用力振荡,然后静置待分层;④分离出乙酸乙酯层,洗涤、干燥.
;③待试管B(内装滴有酚酞的饱和碳酸钠溶液)收集到一定量产物后停止加热,撤去导管并用力振荡,然后静置待分层;④分离出乙酸乙酯层,洗涤、干燥.
此实验甲中B装置导管距离液面一段距离的作用为:防倒吸
此实验防倒吸的原因为:防止b中滴有饱和碳酸氢钠的溶液倒流回热的试管底部,使试管炸裂,同时也防止碳酸钠溶液与乙酸反应,造成产物的损失。
4、蓄液式
【例1】(2022・上海・卢湾高级中学模拟预测)以印刷线路板的碱性蚀刻废液(主要成分为[Cu(NH3)4]Cl2)或焙烧过的铜精炼炉渣(主要成分为CuO、SiO2少量Fe2O3)为原料均能制备CuSO4•5H2O晶体。取一定量蚀刻废液和稍过量的NaOH溶液加入到如图所示实验装置的三颈瓶中,在搅拌下加热反应并通入空气,待产生大量的黑色沉淀时停止反应,趁热过滤、洗涤,得到CuO固体;所得固体经酸溶、结晶、过滤等操作,得到CuSO4•5H2O晶体。
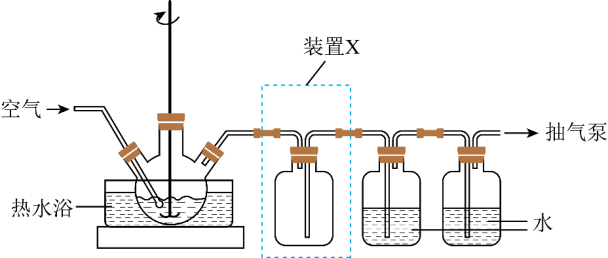
此实验装置x的作用为安全瓶,防倒吸
此实验防倒吸的原因;实验中有氨气生成,氨气极易溶于水,易产生倒吸,此装置可以使倒吸进入的溶液储存于x中,防止进入三颈烧瓶底部,所以装置图中装置x的作用是防止倒吸。
【例2】(2022・安徽・马鞍山二中二模)亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂,可用ClO2为原料制取,装置如图。请回答下列问题:

已知:①饱和NaClO2溶液中析出的晶体成分与温度的关系如下表所示:
温度/℃ | <38 | 38~60 | >60 |
晶体成分 | NaClO2・3H2O | NaClO2 | NaClO2分解成NaClO3和NaCl |
②ClO2极易溶于水,不与水反应,沸点11℃。
此实验中共有三处防倒吸装置,分别为两个倒立式漏斗以及安全瓶
此实验中安全瓶防倒吸的目的为:产生的二氧化氯极易溶于水,防止装置b中的NaOH倒流回装有氯酸钠,亚硫酸钠以及浓硫酸的发生装置中,与其发生反应造成最终产物的减少。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。01 恒压装置 02 防堵塞装置 03 气体(比例)控制器 04 气体(开关)控制器 05 干燥( 洗气 ...
一、冷指冷凝管 传统冷凝管(如直形冷凝管、球形冷凝管、蛇形冷凝管等)用于将气态物...
1.三颈烧瓶: 又称三口烧瓶,用作当溶液长时间的反应,需加热回流的反应容器。三颈圆...
使用启普发生器时需要满足以下条件: 反应物状态:必须是块状固体与液体的反应,而不...
酒精灯和酒精喷灯是实验室常用的加热器具。酒精灯的温度一般可达400~500℃;酒精喷灯...
启普发生器适用于不溶于水的块状(或粒状)固体与液体(或溶液)反应物在常温下的反应,如...