
|
学习小专题 |

|
学习小专题 |
 [注解与辨疑i] 化学反应速率中几个重要的拓展概念 作者:化学自习室 来源:未知 日期:2019-12-18 08:24:05 点击:2619 所属专题:化学反应速率 速率常数 基元反应 活化能
[注解与辨疑i] 化学反应速率中几个重要的拓展概念 作者:化学自习室 来源:未知 日期:2019-12-18 08:24:05 点击:2619 所属专题:化学反应速率 速率常数 基元反应 活化能
在高中阶段研究外界条件对化学反应速率的影响时,教材中出现了基元反应、活化能、反应速率常数等概念。那我们在日常的教学中,如何把握教学的深广度呢? 一、基元反应 原高中教材在讨论反应速率存在一些问题: ⑴学生不了解化学反应是如何进行的,比如 H 2 +Cl 2 =HCl...
 [注解与辨疑i] 如何理解勒沙特列原理中的“压强” 作者:化学自习室 来源:未知 日期:2019-11-27 18:31:33 点击:2302 所属专题:勒沙特列原理盲区
[注解与辨疑i] 如何理解勒沙特列原理中的“压强” 作者:化学自习室 来源:未知 日期:2019-11-27 18:31:33 点击:2302 所属专题:勒沙特列原理盲区
一、问题的提出 勒夏特列原理是化学平衡中的重要经验原理,也是高中阶段学生和教师解决化学平衡问题的主要依据。虽然有研究者认为勒夏特列原理只是经验性总结,只能定性判断,并且在实际应用中有条件限制(包括“均相、封闭体系、只允许一个因素改变等”),不建议向学...
 [注解与辨疑i] 为什么加入氯化钾晶体使三价铁离子和硫氰根离子混合液颜色变浅? 作者:化学自习室 来源:未知 日期:2019-10-06 18:23:10 点击:1630 所属专题:氯化铁
[注解与辨疑i] 为什么加入氯化钾晶体使三价铁离子和硫氰根离子混合液颜色变浅? 作者:化学自习室 来源:未知 日期:2019-10-06 18:23:10 点击:1630 所属专题:氯化铁
Fe 3+ +(n)SCN - Fe(SCN)n (3-n) 从Fe 3+ 和SCN - 反应的离子方程式可以看出,K + 和Cl - 都没有参加反应,加入KCl不会引起Fe 3+ /SCN - 平衡的移动。事实上,加入NaNO 3 、CH 3 COONH 4 、Na 2 SO 4 或KI等这些与平衡无关的强电解质晶体,都会使Fe 3+ /SCN - 溶...
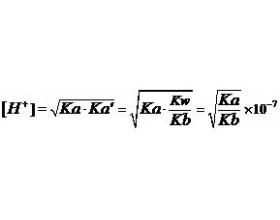 [注解与辨疑i] 有关酸碱性概念的归纳 作者:伍伟夫 来源:化学原理补正 日期:2021-08-16 12:06:00 点击:3514 所属专题:溶液酸碱性
[注解与辨疑i] 有关酸碱性概念的归纳 作者:伍伟夫 来源:化学原理补正 日期:2021-08-16 12:06:00 点击:3514 所属专题:溶液酸碱性
“酸碱性”概念是一个十分重要的,且有多重含义的化学概念。为了使学生能较好地区分“物质酸碱性”与“溶液酸碱性”概念上的不同,有必要在教学中归纳和总结出如下几点,以便让学生对其能有一个更为清楚的认识。 一、物质的酸碱性 酸与碱恐怕是人们最早认识的两类化学物...
 [注解与辨疑i] 如何定量理解越弱越水解? 作者:化学自习室 来源:未知 日期:2019-06-27 15:19:22 点击:1974 所属专题:盐类水解规律 水解平衡常数
[注解与辨疑i] 如何定量理解越弱越水解? 作者:化学自习室 来源:未知 日期:2019-06-27 15:19:22 点击:1974 所属专题:盐类水解规律 水解平衡常数
盐类的水解规律中有“谁弱谁水解,越弱越水解”. 在课本“科学视野”栏目中介绍了盐的水解常数,但很多学生却不够重视,殊不知其推导过程能帮助我们更深入的去理解水解规律. 例1 在25 ℃时,等浓度的NaF 溶液pH=a 和NaCN 溶液的pH=b,则a b(填“>”“<”或“=”)(数...
 [注解与辨疑i] 平衡向体积增大方向移动,混合气体平均相对分子质量一定减小吗? 作者:化学自习室 来源:未知 日期:2019-06-26 10:16:57 点击:1312 所属专题:平衡移动量变
[注解与辨疑i] 平衡向体积增大方向移动,混合气体平均相对分子质量一定减小吗? 作者:化学自习室 来源:未知 日期:2019-06-26 10:16:57 点击:1312 所属专题:平衡移动量变
对于全是气体的化学反应,平衡向扩体方向移动,由于气体的总质量不变,气体的物质的量增大,混合气体的平均相对分子质量将减小. 而对于不全是气体的反应,平衡向扩体方向移动,由于气体的总质量和总物质的量均发生改变,混合气体的平均相对分子质量要具体分析. 例如可逆反应C(s)+H...
 [注解与辨疑i] 平衡向正反应方向移动,生成物的百分含量变化一定增大吗? 作者:化学自习室 来源:未知 日期:2019-06-26 10:09:30 点击:3559 所属专题:平衡移动量变
[注解与辨疑i] 平衡向正反应方向移动,生成物的百分含量变化一定增大吗? 作者:化学自习室 来源:未知 日期:2019-06-26 10:09:30 点击:3559 所属专题:平衡移动量变
若是通过改变压强或温度使平衡向正反应方向移动,则生成物的百分含量一定会增大. 若平衡是由于加入反应物而发生移动,如反应2SO 2 (g)+O 2 (g) 2SO 3 (g)达平衡状态时,保持其它条件不变,加入一定量的SO 2 (或O 2 ),则达新平衡时,SO 3 的百分含量可能增大也可能减小,这...
 [注解与辨疑i] 平衡发生移动时,各反应物转化率的变化分析 作者:化学自习室 来源:未知 日期:2019-06-26 10:05:37 点击:1619 所属专题:平衡移动量变
[注解与辨疑i] 平衡发生移动时,各反应物转化率的变化分析 作者:化学自习室 来源:未知 日期:2019-06-26 10:05:37 点击:1619 所属专题:平衡移动量变
转化率是指在一定条什下,某可逆反应达到平衡时,某反应物转化的浓度占该反应物起始浓度的百分率. 转化率=(C 始 -C 终 )÷ C 始 × 100% 因此,凡是能引起化学平衡移动的因素,都可使某反应物的转化率发生变化,至于平衡发生移动时反应物的转化率如何变化,则要根据 具体反应进...
 [注解与辨疑i] 有气体参加(或生成)的平衡体系中, 再充入气体对平衡的影响分析 作者:化学自习室 来源:未知 日期:2019-06-26 10:00:58 点击:1934 所属专题:惰性气体影响
[注解与辨疑i] 有气体参加(或生成)的平衡体系中, 再充入气体对平衡的影响分析 作者:化学自习室 来源:未知 日期:2019-06-26 10:00:58 点击:1934 所属专题:惰性气体影响
1.加入与反应相关的气体 (1)在容积恒定的密闭容器中,反应已达平衡,此时只要充入反应体系中任何一种气体,也就是改变反应体系中任何一种气体的浓度, 平衡都会发生移动.平衡移动的方向应从浓度对平衡的影响来判断,而不应从压强的影响去判断. 例如:2SO 2 (g)+O 2 (g) 2SO...
 [注解与辨疑i] 等体积反应,化学平衡发生移动时压强是否一定不变? 作者:化学自习室 来源:未知 日期:2019-06-26 09:57:51 点击:1541 所属专题:平衡移动量变
[注解与辨疑i] 等体积反应,化学平衡发生移动时压强是否一定不变? 作者:化学自习室 来源:未知 日期:2019-06-26 09:57:51 点击:1541 所属专题:平衡移动量变
通常情况下压强对化学平衡的影响是指反应在体系内外可进行能量传递的容器中进行的,在这一前提下的等体反应,压强保持恒定时,不能作为判断化学平衡的标志,化学平衡发生移动时压强也保持恒定. 但如果反应是在一个体积不变的绝热容器中的等体反应,压强保持恒定时,可作为判断化学...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。1.无论是用某一反应物表示还是用某一生成物表示,由于Δ C 是取浓度变化的绝对值,因...
在一个恒温恒容的密闭容器里,充入2mol SO 2 和1mol O 2 ,发生如下反应并建立化学平...
...
一、人物简介: 阿伦尼乌斯·斯万特·奥古斯特(1859年2月19日~1927年10月2日)瑞典物...
本题考查了阿伦尼乌斯公式中温度和速率常数的关系,即温度升高,速率常数变大。 本题...
工业生产中适宜生产条件的选择原则 : (1)从化学反应速率分析:既不能过快,也不能...
化学反应总是在一定条件下进行。化学反应速率和化学平衡从两个角度诠释了反应进行的两...
问题一:根据合成氨的反应方程式, N 2 和 H 2 物质的量之比为 1 ﹕ 3 ,但实际生产中...