|
乙醇・知识点精析・乙醇的化学性质
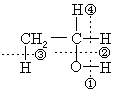
要抓住羟基的结构特点以及乙基和羟基的相互影响来理解、掌握乙醇的化学性质。 在乙醇分子中O―H键,C―O键,C―H键都是极性键,在一定条件下可发生如下四种情况的键的断裂
(1)乙醇跟钠反应时,按①式断裂,发生置换反应生成CH3CH2ONa,同时放出H2。 (2)乙醇跟溴化氢反应时,按②式断裂,发生取代反应生成CH3CH2Br和H2O。 (3)在醇的催化氧化反应中,醇分子中断裂的是①O―H键和④C―
可见能发生催化氧化反应的醇,其必备的结构条件是:连有―OH的碳原子上必须要有氢原子。因此,如 乙醇在加热和有催化剂(Cu或Ag)的条件下,能被空气中的氧气氧化成乙醛,其反应实质是:2Cu+O2
(4)醇的脱水反应较复杂,有分子内脱水和分子间脱水两种情况。当分子内脱水时断裂的是②C―O键和③C―H键,发生消去反应生成
由此可见,能发生消去反应的醇必备的结构条件是连有―OH的碳原子的相邻碳原子上必须有氢原子,因此CH3―OH、 醇的分子间脱水是一个醇的分子断裂①O―H键,另一个醇分子断裂②C―O键,发生取代反应生成乙醚和H2O
|
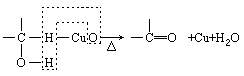
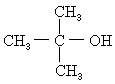 等醇就不能发生催化氧化反应。
等醇就不能发生催化氧化反应。
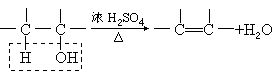
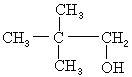 等均不能发生消去反应生成不饱和化合物。这一点与醇的催化氧化不同,初学者特别容易混淆,希望学生仔细加以比较、区别。
等均不能发生消去反应生成不饱和化合物。这一点与醇的催化氧化不同,初学者特别容易混淆,希望学生仔细加以比较、区别。