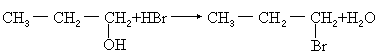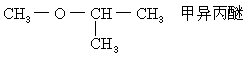| 乙醇・典型题剖析
例1 下列关于1-丙醇的叙述中,正确的是 [ ] A.1-丙醇与氧气的混合气体通过赤热的铜,生成丙醛 B.1-丙醇不能和氢卤酸发生反应 C.1-丙醇的沸点高于乙醇 D.1-丙醇、2-丙醇、丙醚互为同分异构体 分析 在铜或银催化作用下,醇和O2反应欲生成醛,醇分子中与―OH相连的碳原子上必需有两个氢原子,1-丙醇满足此条件,其氧化后能生成醛:
1-丙醇能和氢溴酸反应,C―O键断裂,溴原子取代羟基,生成1-溴丙烷。反应方程式如下:
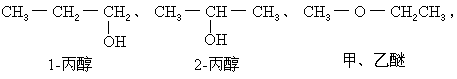
B错误。 乙醇、1-丙醇是同系物,结构和性质相似,1-丙醇分子量大,因此分子间作用力大于乙醇,沸点高于乙醇。C正确。 丙醇的分子式为C3H8O,其同分异构体为:
而丙醚的分子式为C6H14O,显然D是错误的。 答 A、C。 例2 相同质量的下列醇,分别与过量的钠反应,放出氢气最多的是_____,最少的是 [ ] A.甲醇 B.乙醇 C.乙二醇 D.丙三醇 分析 等质量的醇分别与足量钠反应,放出氢气的多少,取决于等质量的不同醇提供羟基数的多少,mg上述物质所含羟基的物质的量分
以等质量的上述醇,丙三醇与钠反应产生的氢气最多,乙醇与钠反应产生的氢气最少。 答 D、B。 例3 0.2mol有机物和1.2mol O2在一密闭容器中恰好完全燃烧,产物依次通过浓H2SO4、碱石灰。浓H2SO4的质量增加18g,碱石灰固体质量增加35.2g,通过计算回答: (1)此有机物的分子式。 (2)它可能有的同分异构体共有多少种? (3)若该有机物能与金属钠反应放出H2气,且该有机物不能发生催化氧化反应,写出该有机物的结构简式并命名。 分析 该有机物燃烧后只生成CO2和H2O,因此该有机物可能为烃或烃的含氧衍生物。0.2mol有机物分子中含氧原子物质的量为生成的CO2所含氧原子物质的量,加上燃烧生成水中所含氧原子物质的量,减去燃烧时所需O2中氧原子物质的量,并由此求出有机物的化学式。然后根据化学式按官能团异构-碳链异构-位置异构的顺序考虑所有的同分异构体。最后根据已知物质的化学性质去推断该有机物的可能结构简式。
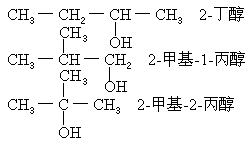
0.2mol有机物中含氧原子物质的量=0.8mol×2+1mol-1.2mol×2=0.2mol 即0.2mol有机物中含0.8mol碳原子,2mol氢原子,0.2mol氧原子。 所以化学式为C4H10O,符合CnH2n+2O通式,可能为饱和一元醇或醚。 (2)其同分异构体为: CH3―CH2―CH2―CH2―OH 1-丁醇
CH3―O―CH2CH2CH3 甲丙醚
CH3―CH2―O―CH2CH3 乙醚 (3)由于该有机物能与金属钠反应放出H2,且不能发生催化氧化反应,因此该有机物只能为2-甲基-2-丙醇。 |