
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
1、为什么硫矿多出现在火山口咐近?
任何矿物的形成都和火山、地震、流水冲刷沉积等地壳活动有关,我们知道,火山口喷出的气体里常含有大量H2S。H2S气体一旦进入氧化性气氛的大气 中,很容易被空气中的O2氧化为S:2H2S+O2= 2H2O + 2S,目前,一些火山活动比较多的国家和地 区,还有不少直接在火山口附近直接采集硫磺的现象,在一些火山口附近的地表通过上述氧化反应沉积的硫磺层,遭遇新的剧烈火山活动或地震时,则可能再次被覆盖埋入地下,形成硫磺的矿床。
2、如何开釆地下硫矿?
很多人可能觉得,这还不简单,跟挖煤一样打一 矿井,派人下去开釆不就得了,其实不需要如此麻烦。科学家根据硫单质的熔点只有113°C,设计了一个非 常巧妙的方案:在硫磺矿上方钻一机井直达矿床,通 过管道向井下输入过热水蒸气(如150 °C),硫磺受热熔化后,通过机器即可像抽水一样将熔化的硫抽出, 注入冷水中冷却,即得固体硫磺。
3、为什么天然气中往往含有H2S气体?地球表面每天那么多动植物遗体不断腐败,为什么大气成分里不 含有H2S气体?
要回答这个问题,首先我们要知道天然气的来历,一般认为,天然气和石油、煤一样,是由古代地壳运动中埋藏到地下的有机质(动、植物遗体)在缺氧条件下产生的,所以天然气、煤、石油并称“化石燃料”,动植物体内的硫元素(大多数蛋白质是含硫的)在形成天然气的还原性条件下即转化为H2S。
地球表面的动、植物遗体在不断腐败,产生H2S 气体,这也正是沼气池、化粪池、下水道等封闭的发酵设施逸出的气体具有臭味的主要原因。但是,逸出到大气中的H2S“寿命”不会长久,很快就被O2氧化掉, 所以大气的成分里几乎不含有H2S气体。
4、维修工人进入下水道前,应该如何防止H2S气体 中毒?
这是一个非常现实的问题,其实不仅下水道维修,沼气池、化粪池等设施的维护维修都涉及防止 H2S中毒的问题。因缺乏防护意识、不懂防护措施,误 入上述设施中毒甚至直接死亡的案例,几乎每年都有报道。
作为学习化学的你,可能根据H2S的性质想到诸如用碱中和、用氧化剂氧化等过于复杂的办法,其实很简单,只需要一台鼓风机即可。因为上述封闭设施内不仅仅有H2S,更多的是CH4,N2等不支持呼吸的气体,用鼓风机将大量新鲜空气送入,将CH4、H2S、 N2等气体吹出即可解决问题。
5、一般情况下都是强酸制弱酸,为什么H2S(弱酸) 通入CuSO4溶液可制得硫酸(强酸):H2S + CuSO4= CuS ↓ +H2SO4?
这个问题还可以从别的角度提出,比如为什么同样是弱酸(H2S)的盐,FeS可以与硫酸反应:FeS + H2SO4= FeSO4+H2S ↑ ,而CuS则不能与硫酸反应?
说简单也很简单,其实大部分都是由于CuS溶解度太小的缘故。
CuS这种物质在水中的溶解度极小(也可以说溶度积常数ksp极小),在Cu2+一定的条件下,只需要物质的量浓度极低的 S2- 即可从溶液中析出CuS沉淀。H2S是二元弱酸,需经过2步电离才能产生浓度极低 的 S2- (饱和H2S溶液中,S2- 的物质的量浓度浓度约 为7×10-15mol/L),但这对于沉淀 Cu2+ 来说已经足够了(Ksp(CuS)为6×10-36,这个数据告诉我们,对 于0.1 mol/L的CuSO4溶液,只需要有6 ×10-35 mol/L的量就可以产生CuS沉淀),H2S气体通 入一定浓度的铜盐溶液时,随着CuS沉淀不断析出, H2S也不断电离,最终形成“弱酸制强酸”的结果。
通过上述分析不难发现,“弱酸制强酸”只是表观的现象,生成极其难溶的CuS沉淀才是反应的本质。
与CuS相比,同样不溶解于水的FeS就不同了, Ksp(FeS)为10-17量级,单从这个数据看,似乎在饱和 H2S溶液(可以电离产生10-15mol/L的 S2- )里加 入一定浓度的 Fe2+,也符合形成 FeS 沉淀的要求,但是我们要看到,随着微量 FeS(尚不能形成肉眼可见的沉淀程度)的形成,体系内就会因为 H2S 电离产生较高浓度的H+,抑制H2S,HS-等的电离,这时溶液里的 S2- 的物质的量浓度不可能达到单独 H2S 饱和溶液时的10-15mol/L,也就是说,H2S不可能与 Fe2+盐溶液持续反应形成FeS沉淀。
以上只是定性、直观的理解,其实我们完全可以从平衡常数的角度对以上过程加以分析。
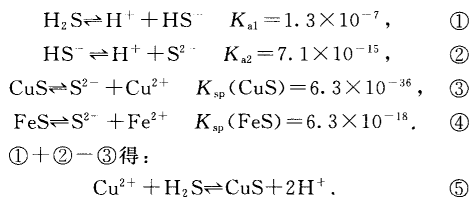
根据平衡常数的性质可得,反应⑤的平衡常数
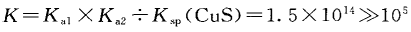
可见该反应属于完全的自发反应,同样方法计算反应 Fe2++H2S=FeS+2H+ 的平衡常数:
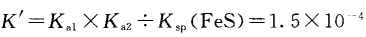
该数值非常之小,接近10-5数量级,说明该反应只有极其微弱的可逆性,以至于我们很难观察到反应的发生。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
一、认识双氧水:从分子结构说起 化学名称:过氧化氢(Hydro...
一、总方法:接触法 整个工业制硫酸分为三个阶段、三个设备、...
1.硫代硫酸钠(Na 2 S 2 O 3 ): Na 2 S 2 O 3 ·5H 2 O俗名海波或大苏打,...
...
磷作为周期表第 ⅤA 族核心元素,兼具 “生命不可替代性”(构...
硫酸盐 俗名 颜色 用途 2CaSO 4 H 2 O 熟石膏 白色 CaSO 4 2H 2 O 生石膏...