
|
学习小专题 |

|
学习小专题 |
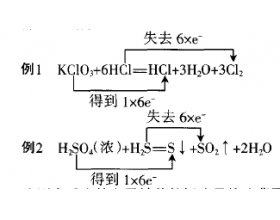 [方法与规律y] 电子转移数目容易标错的氧化还原反应 作者:周书峰 来源:濮阳市油田三高 日期:2016-03-27 10:38:05 点击:1342 所属专题:电子转移数目
[方法与规律y] 电子转移数目容易标错的氧化还原反应 作者:周书峰 来源:濮阳市油田三高 日期:2016-03-27 10:38:05 点击:1342 所属专题:电子转移数目
氧化还原反应是高中化学教学的重点之一,多 年来高考都十分重视对这部分知识的考査。考纲要 求“了解氧化还原反应的本质是电子转移,了解常见的氧化还原反应。”其中关于电子转移数目的计算是 高考命题的常见题型。 笔者在教学中发现,学生最容易出现的错误集中在某几类反应...
 [方法与规律y] 氧化还原反应电子转移数目的判断 作者:武群 来源:未知 日期:2016-03-25 10:58:43 点击:6776 所属专题:电子转移数目 双线桥法
[方法与规律y] 氧化还原反应电子转移数目的判断 作者:武群 来源:未知 日期:2016-03-25 10:58:43 点击:6776 所属专题:电子转移数目 双线桥法
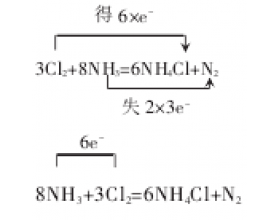
氧化还原反应电子转移电子数目的判断,一直是困扰许多学生的一个难点,根据自己多年的教学经验,特总结如下: 对于双箭桥表示法,电子转移数表示为:A×B e - 形式, 其中 A为反应前后化合价变化的原子个数;B=高价态—低价态,A=1 或B=1 将 省略 对于单箭桥表示法,电子转...
 [方法与规律y] 怎样分析竞争反应的先后? 作者:张瀚 来源:未知 日期:2015-01-28 16:04:13 点击:2251 所属专题:反应先后
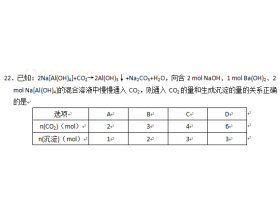
[方法与规律y] 怎样分析竞争反应的先后? 作者:张瀚 来源:未知 日期:2015-01-28 16:04:13 点击:2251 所属专题:反应先后
答案 :反应顺序为:先碳酸钡,再碳酸钠;再氢氧化铝;再碳酸氢钠,再碳酸氢钡。 解析 :氢氧根和二氧化碳先反应,生成碳酸根的同时就和钡离子反应了,这个反应总起来就相当于和氢氧化钡反应了,至于是谁的氢氧根无所谓了。 总结 : 像这种竞争反应的先后问题,理科的思...
 [方法与规律y] 氧化还原反应6大规律 作者:鲁志超 来源:未知 日期:2014-12-06 22:43:13 点击:1448 所属专题:氧化还原反应规律
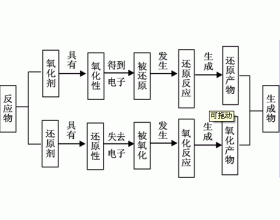
[方法与规律y] 氧化还原反应6大规律 作者:鲁志超 来源:未知 日期:2014-12-06 22:43:13 点击:1448 所属专题:氧化还原反应规律
高中化学氧化还原反应是一类非常重要的反应,是指元素化合价在反应前后有变化的化学反应,微观上是有电子转移或偏移的反应。在氧化还原反应中有许多规律,这里进行简单的总结。 1、守恒规律 守恒是氧化还原反应最重要的规律。在氧化还原反应中,元素的化合价有升必有降,电...
 [方法与规律y] 氧化还原反应常用的几种配平方法 作者:徐俊龙 来源:未知 日期:2014-09-12 08:29:24 点击:1994 所属专题:氧化还原反应配平
[方法与规律y] 氧化还原反应常用的几种配平方法 作者:徐俊龙 来源:未知 日期:2014-09-12 08:29:24 点击:1994 所属专题:氧化还原反应配平
...
 [方法与规律y] “四步法”书写陌生氧化还原反应方程式 作者:张瀚 来源:未知 日期:2014-05-07 15:12:34 点击:2985 所属专题:氧化还原反应方程式 陌生方程式
[方法与规律y] “四步法”书写陌生氧化还原反应方程式 作者:张瀚 来源:未知 日期:2014-05-07 15:12:34 点击:2985 所属专题:氧化还原反应方程式 陌生方程式
一、陌生氧化还原反应方程式的书写方法 1.“四步法”书写陌生氧化还原反应方程式 第一步:根据元素化合价的升降判断氧化剂、还原剂、氧化产物、还原产物。 第二步:按“氧化剂+还原剂=还原产物+氧化产物”写出方程式,根据得失电子守恒配平上述四种物质。注意:不属于“...
 [方法与规律y] 氧化还原离子方程式配平及训练 作者:张瀚 来源:未知 日期:2013-02-27 11:32:35 点击:6463 所属专题:氧化还原反应配平 离子方程式配平
[方法与规律y] 氧化还原离子方程式配平及训练 作者:张瀚 来源:未知 日期:2013-02-27 11:32:35 点击:6463 所属专题:氧化还原反应配平 离子方程式配平
氧化还原离子方程配平步骤: 1、判断产物 2、双线桥(降价线桥必须在上方) 3、变价元素守恒(针对反应物) 4、仅对Na2O2适用(补全钠离子) 5、用氢离子/氢氧根调平方程 6、用水调平氢 【简单氧化还原反应离子方程书写】 ①KMnO 4 +Na 2 S溶液 酸性条件 碱性条件 ②KMnO 4...
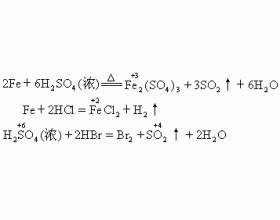 [方法与规律y] 氧化产物和还原产物的判断 作者:潘祥泰 来源:未知 日期:2016-03-09 18:31:22 点击:13625 所属专题:氧化还原反应方程式 氧化产物 还原产物
[方法与规律y] 氧化产物和还原产物的判断 作者:潘祥泰 来源:未知 日期:2016-03-09 18:31:22 点击:13625 所属专题:氧化还原反应方程式 氧化产物 还原产物
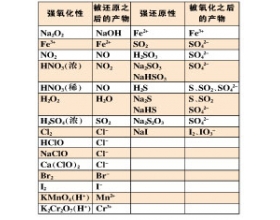
判断氧化产物和还原产物时,应抓住变价元素化合价的特征。当还原剂或氧化剂中所含变价元素的升降只存在一种可能时,它们的产物易于判断: ①非金属单质作氧化剂时,化合价变为负价(一般只有一个)。如,卤素由0价变为-1价,氧族元素由0价变为-2价,氮、磷由0价变为-3价...
 [方法与规律y] 氧化还原反应方程式配平的程序与技巧 作者:江已舒 来源:未知 日期:2014-11-03 11:01:42 点击:8484 所属专题:氧化还原反应配平
[方法与规律y] 氧化还原反应方程式配平的程序与技巧 作者:江已舒 来源:未知 日期:2014-11-03 11:01:42 点击:8484 所属专题:氧化还原反应配平
氧化还原反应方程式的配平原理很简单,但初学者在配平过程 中往往感到较困难,其实只要解决好配平的程序,配平起来就比较简单了。 一配平的关键 -先确定什么物质的计量数 若(1)氧化剂、还原剂(简称两剂)是两种不同的物质且均全部被还原、被氧化,则应首先确定两剂的计...
 [方法与规律y] 复杂氧化还原反应离子方程式 作者:周广 来源:未知 日期:2012-03-07 11:49:44 点击:22161 所属专题:离子方程式书写 氧化还原反应方程式
[方法与规律y] 复杂氧化还原反应离子方程式 作者:周广 来源:未知 日期:2012-03-07 11:49:44 点击:22161 所属专题:离子方程式书写 氧化还原反应方程式
高中化学涉及的反应是以氧化还原反应为主题,又经常以离子方程式的形式来体现,在高考题中经常涉及的一些复杂氧化还原反应离子方程式的书写,对于高三学生来讲往往是一道不可逾越的墙,究竟有没有一种可行有效的方法解决这个问题呢?笔者通过对众多氧化还原反应的离子方...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。说明: 1.不同于大学所说的“氧化数”,高中所学的“化合价”只是一个工具,是为了更...
氧化还原反应的很多规律,如化合价有升必有降、电子有得必有失,而且升降总数相等、得...
配平氧化还原反应方程式的基本方法相同,关键是针对具体的反应往往有不同的配平技巧。...
氧化性、还原性的强弱主要取决于物质本身得失电子的难易程度而不取决于得失电子数目的...
得失电子守恒是氧化还原反应的核心,根据这一原理,既可配平氧化还原方程式,又可进行...
1 问题的提出 “氧化还原反应”在中学化学知识中占据着关键性位置,是电化学的基础,...
陌生氧还反应书写步骤: 陌生方程式书写 找出“两剂两产物” 根据已知信息找到并写出...
对于有很多种物质参与的复杂氧化还原反应来说,观察法很难直接配平。 这时,我们可以...