
|
学习小专题 |

|
学习小专题 |
 [注解与辨疑y] 有关氧化还原反应的易错判断 作者:杨帆 来源:未知 日期:2014-06-09 15:53:20 点击:710 所属专题:氧化还原反应 是非判断
[注解与辨疑y] 有关氧化还原反应的易错判断 作者:杨帆 来源:未知 日期:2014-06-09 15:53:20 点击:710 所属专题:氧化还原反应 是非判断
( )1. 有单质参加或有单质生成的反应一定是氧化还原反应。 ( )2. 为了防止中秋月饼等富脂食品氧化变质常在包装袋中放入硫酸亚铁。 ( )3. 为了增强高锰酸钾的氧化能力,可用浓盐酸对高锰酸钾溶液进行酸化。 ( )4. 向含有少量FeBr 2 的FeCl 2 溶液中加入适量氯水...
 [注解与辨疑y] 中学化学中的歧化反应与归中反应 作者:刘明 来源:未知 日期:2014-05-27 11:32:57 点击:1313 所属专题:歧化反应 归中反应
[注解与辨疑y] 中学化学中的歧化反应与归中反应 作者:刘明 来源:未知 日期:2014-05-27 11:32:57 点击:1313 所属专题:歧化反应 归中反应
...
 [注解与辨疑y] 解读十类化学竟争反应 作者:孙法军 来源:未知 日期:2016-01-17 20:32:55 点击:1346 所属专题:反应先后
[注解与辨疑y] 解读十类化学竟争反应 作者:孙法军 来源:未知 日期:2016-01-17 20:32:55 点击:1346 所属专题:反应先后
现行中学教材中,涉及到十种类型的反应需要考虑到试剂反应的先后顺序,现列举如下。 1、酸性不同的酸遇同一种碱 当同一溶液中存在多种酸时,若向此溶液中逐滴加入一种碱液时,一般来说,碱先与酸性强的酸反应,然后与酸性较弱的酸的反应。如向盐酸和醋酸的混合溶液逐滴...
 [注解与辨疑y] 物质的氧化性、还原性辨析 作者:张玮 来源:未知 日期:2016-01-17 16:50:02 点击:1645 所属专题:氧化性 还原性
[注解与辨疑y] 物质的氧化性、还原性辨析 作者:张玮 来源:未知 日期:2016-01-17 16:50:02 点击:1645 所属专题:氧化性 还原性
氧化剂易于得到电子,具有氧化性。还原剂易于失去电子,具有还原性。所谓氧化性,是指具有氧化别的元素的能力,即夺取电子的能力;还原性是指具有还原别的元素的能力,即失去电子的能力。一般地说,强氧化剂,它的氧化性强,自身易被还原;强还原剂,它的还原性强,自身...
 [注解与辨疑y] 氧化还原反应电子转移的表示方法 作者:黄瑞 来源:未知 日期:2014-10-31 21:35:26 点击:5445 所属专题:双线桥法
[注解与辨疑y] 氧化还原反应电子转移的表示方法 作者:黄瑞 来源:未知 日期:2014-10-31 21:35:26 点击:5445 所属专题:双线桥法
1.双线桥法。 (1)两条桥线从反应物指向生成物,且对准同种元素; (2)要标明“得”“失”电子,且数目要相等; (3)箭头不代表电子转移的方向。 一般在线桥上可不标明化合价的升降, 2.单线桥法。 (1)一条桥线表示不同元素原子得失电子的情况;; (2)不需标明“得”“失”电...
 [注解与辨疑y] 常见阴离子还原性强弱顺序 作者:袁建标 来源:未知 日期:2022-08-29 16:26:40 点击:42000 所属专题:还原性
[注解与辨疑y] 常见阴离子还原性强弱顺序 作者:袁建标 来源:未知 日期:2022-08-29 16:26:40 点击:42000 所属专题:还原性
常见阴离子还原性强弱顺序:S 2- SO 3 2- I - Fe 2+ Br - Cl - OH - 含氧酸根 F - 最常用的四种离子的还原性强弱顺序为:亚铁离子Fe 2+ <碘离子I - <亚硫酸根离子SO 3 2- <硫离子S 2- 依据 : 2Fe 3+ + 2I - =2Fe 2+ + I 2 SO 3 2- +I 2 + H 2 O = SO 4 2- +2I - + 2H...
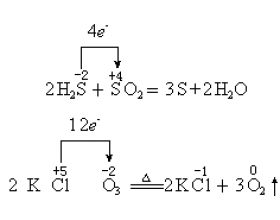 [注解与辨疑y] 氧化还原反应的表示法:单线桥和双线桥解析 作者:彭中游 来源:未知 日期:2016-01-17 20:34:51 点击:110996 所属专题:双线桥法
[注解与辨疑y] 氧化还原反应的表示法:单线桥和双线桥解析 作者:彭中游 来源:未知 日期:2016-01-17 20:34:51 点击:110996 所属专题:双线桥法
氧化还原反应中电子转移情况有两种表示法:单线桥和双线桥。 (1) 单线桥(也叫单箭号) 意义:表示电子转移的方向和总数(或:表示不同元素原子或离子间电子得失情况)。它体现了谁给谁。 表示法:箭号一定在等式左边,箭头上只标明电子转移总数。如: 该表示法的特点是:箭...
 [注解与辨疑y] 高中化学归中反应知多少 作者:赵亭 来源:未知 日期:2013-03-01 14:55:49 点击:8020 所属专题:归中反应
[注解与辨疑y] 高中化学归中反应知多少 作者:赵亭 来源:未知 日期:2013-03-01 14:55:49 点击:8020 所属专题:归中反应
归中反应指的是含有同种元素的不同价态的两种物质发生氧化还原反应,生成只含有该元素中间价态的物质的反应。发生归中反应的条件是要符合中间价态理论:含有同种元素的不同价态的两种物质,只有当这种元素有中间价态时,才有可能发生归中反应。归中反应的特点是氧化产物和还...
 [注解与辨疑y] 高中化学歧化反应知多少 作者:许浩年 来源:未知 日期:2013-03-01 14:52:57 点击:20480 所属专题:歧化反应
[注解与辨疑y] 高中化学歧化反应知多少 作者:许浩年 来源:未知 日期:2013-03-01 14:52:57 点击:20480 所属专题:歧化反应
歧化反应指的是同一物质的分子中同一价态的同一元素间发生的氧化―还原反应。即该元素的原子(或离子)一部分被氧化,另一部分被还原,是自身氧化还原反应中的一种。歧化反应的特点是氧化剂和还原剂是同一种物质。 1.过氧化钠或超氧化钾等分别与二氧化碳、水反应(过氧化钠可...
 [注解与辨疑y] 中学常见的氧化还原反应 作者:乔梁 来源:未知 日期:2019-01-08 08:58:41 点击:11162 所属专题:氧化还原反应
[注解与辨疑y] 中学常见的氧化还原反应 作者:乔梁 来源:未知 日期:2019-01-08 08:58:41 点击:11162 所属专题:氧化还原反应
一 . 因氧化还原而不能共存的离子 1. 不需要酸性条件的 MnO 4 - 与 S 2 - 、 Fe 2+ 、 I - 、 SO 3 2 - 、 HS - 、 HSO 3 - 、 S 2 O 3 2 - 、 Sn 2+ 、 H 2 O 2 ; Fe 3+ 与 I - 、 S 2 - 、 HS - 、 SO 3 2 - 、 Sn 2+ 、 HSO 3 - ; ClO - 与 S 2 - 、...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。化合价 化合价是一种元素的一个原子与其他元素的原子化合【即构成化合物】时表现出来...
氧化剂 还原剂 活泼非金属单质:X 2 、O 2 、S 活泼金属单质:Na、Mg、Al、Zn、Fe 某...
常见阴离子还原性强弱顺序:S 2- SO 3 2- I - Fe 2+ Br - Cl - OH - 含氧酸根 F - 最常...
1. 得电子物质被还原是氧化剂。 2. 失e物质、被还原、发生了还原反应。 3. 氧化剂...
常见的强氧化剂简介 具有强烈氧化性的物质。在标准电位顺序中的位置越靠后,标准电位...
非金属单质氧化性: 一般情况下元素非金属性强的对应的单质氧化性强。 例如:非金属性...
氧化还原反应是一类重要的化学反应,其中蕴涵 着“对立统一”等哲学思想.氧化还原反应...
以下几类特殊的氧化还原反应在教与学中值得专题讨论: 一、部分氧化还原反应 在氧化还...