
|
学习小专题 |

|
学习小专题 |
 [物质结构与性质综合] 物质结构说理题汇总 作者:化学自习室 来源:未知 日期:2020-02-24 14:41:28 点击:2883 所属专题:物质结构说理题
[物质结构与性质综合] 物质结构说理题汇总 作者:化学自习室 来源:未知 日期:2020-02-24 14:41:28 点击:2883 所属专题:物质结构说理题
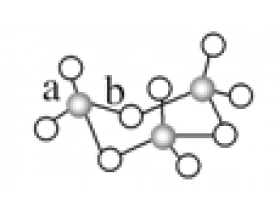
1 、氮原子间能形成氮氮叁键,而砷原子间不易形成叁键的原因是 砷原子半径较大,原子间形成的 σ 键较长 ,p-p 轨道肩并肩重叠程度较小或几乎不能重叠,难以形成 π 键。 AsH 3 分子为三角锥形,键角为 91.80° ,小于氨分子键角 107°,AsH 3 分子键角较小的原因是 砷原...
 [物质结构与性质综合] 物质结构说理题之原子结构问题 作者:化学自习室 来源:未知 日期:2020-02-24 14:41:53 点击:4116 所属专题:物质结构说理题 原子结构03
[物质结构与性质综合] 物质结构说理题之原子结构问题 作者:化学自习室 来源:未知 日期:2020-02-24 14:41:53 点击:4116 所属专题:物质结构说理题 原子结构03
1、稳定性H 2 S>H 2 Se的原因是: 【答】H键的键能比Se-H键的键能大。 2、焰色反应发生的原因为: 【答】激发态电子向基态跃迁,能量以光的形式释放(发射光谱)。 3、检验K元素的方法是焰色反应,请用原子结构的知识解释产生此现象的原因: 【答】当基态原子的电子吸...
 [物质结构与性质综合] 物质结构说理题之核外电子排布问题 作者:化学自习室 来源:未知 日期:2020-02-24 14:42:19 点击:1536 所属专题:物质结构说理题 核外电子排布
[物质结构与性质综合] 物质结构说理题之核外电子排布问题 作者:化学自习室 来源:未知 日期:2020-02-24 14:42:19 点击:1536 所属专题:物质结构说理题 核外电子排布
1、氧元素的第一电离能小于氮元素,原因是: 【答】氮原子的2p轨道处于较稳定的半充满状态而氧原子的不是,氧原子的原子核对电子的吸引能力弱于氟离子。 2、尿素[CO(NH 2 ) 2 ]分子中N、O元素的第一电离能NO,原因是: 【答】N元素的2P能级为半充满,是较稳定的结构,失...
 [物质结构与性质综合] 物质结构说理题之键角问题 作者:化学自习室 来源:未知 日期:2020-02-24 14:42:49 点击:4179 所属专题:物质结构说理题 键角
[物质结构与性质综合] 物质结构说理题之键角问题 作者:化学自习室 来源:未知 日期:2020-02-24 14:42:49 点击:4179 所属专题:物质结构说理题 键角
1、CH 4 的键角大于NH 3 的原因为: 【答】CH 4 中都是C-H单键,键与键之间的排斥力一样,所以是正四面体109.5度,而NH 3 有未成键的孤对电子,孤对电子间的排斥力>孤对电子对化学键的排斥力>化学键间的排斥力,所以由于孤对电子的排斥,键角要小于没有孤对电子排斥...
 [物质结构与性质综合] 物质结构说理题之溶解性问题 作者:化学自习室 来源:未知 日期:2020-03-27 13:32:16 点击:1819 所属专题:物质结构说理题 分子溶解性
[物质结构与性质综合] 物质结构说理题之溶解性问题 作者:化学自习室 来源:未知 日期:2020-03-27 13:32:16 点击:1819 所属专题:物质结构说理题 分子溶解性
1、氨气极易溶于水的原因为: 【答】氨气和水都是极性分子,相似相溶;氨气与水分子间能形成氢键。 2、水由液体形成固体后密度却减小,原因为: 【答】水在形成晶体时,由于氢键的作用使分子间距离增大,空间利用率降低,密度减...
 [物质结构与性质综合] 物质结构说理题之熔沸点问题 作者:化学自习室 来源:未知 日期:2020-02-24 14:43:29 点击:4440 所属专题:物质结构说理题 熔沸点
[物质结构与性质综合] 物质结构说理题之熔沸点问题 作者:化学自习室 来源:未知 日期:2020-02-24 14:43:29 点击:4440 所属专题:物质结构说理题 熔沸点
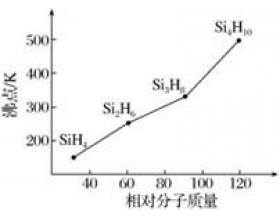
1、氯化铝的熔点为190℃,而氟化铝的熔点为1290℃,导致这种差异的原因为 【答】AlCl 3 是分子晶体,而AlF 3 是离子晶体。 2、P 4 O 10 的沸点明显高于P 4 O 6 ,原因是: 【答】都是分子晶体,P 4 O 10 的分子间作用力高于P 4 O 6 3、H 2 S熔点为-85.5℃,而与其具有...
 [物质结构与性质综合] 《物质结构与性质》基本概念是非判断 作者:化学自习室 来源:未知 日期:2019-11-06 11:38:24 点击:1514 所属专题:物质结构与性质 基本概念 是非判断
[物质结构与性质综合] 《物质结构与性质》基本概念是非判断 作者:化学自习室 来源:未知 日期:2019-11-06 11:38:24 点击:1514 所属专题:物质结构与性质 基本概念 是非判断
一、原子结构与核外电子排布 1. 电子排布1s 2 2s 2 2p 3 3s 1 原子处于基态 2. 可能存在基态核外电子排布式为1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 4p 5 的原子 3. 任何一个能层最多只有s、p、d、f四个能级 4. 6 C的电子排布式1s 2 2s 2 2px 2 反了洪特规则 5. 电子排布式( 21 Sc)...
 [物质结构与性质综合] 思维导图系列3:物质结构 作者:化学自习室 来源:未知 日期:2019-08-04 15:48:41 点击:2935 所属专题:物质结构与性质 物质结构必须
[物质结构与性质综合] 思维导图系列3:物质结构 作者:化学自习室 来源:未知 日期:2019-08-04 15:48:41 点击:2935 所属专题:物质结构与性质 物质结构必须
...
 [物质结构与性质综合] 回归课本之《物质结构与性质》 作者:张劲辉 来源:未知 日期:2019-05-20 10:25:10 点击:1003 所属专题:回归课本 物质结构与性质
[物质结构与性质综合] 回归课本之《物质结构与性质》 作者:张劲辉 来源:未知 日期:2019-05-20 10:25:10 点击:1003 所属专题:回归课本 物质结构与性质
第一章:原子结构与性质 P 1 人类对原子结构的认识发展过程。 P 4 能层即电子层。分别用K、L、M、N、O、P、Q表示。每一个能层分为不同的能级,能级符号用s、p、d、f表示,分别对应1、3、5、7个轨道。能级数=能层序数。 P 7 基态与激发态。焰色反应是原子核外电子从激发态回...
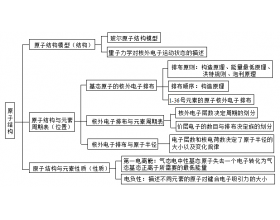 [物质结构与性质综合] 学法指导:《物质结构与性质》图片复习法 作者:吴乾环 来源:未知 日期:2020-03-05 12:42:30 点击:1369 所属专题:物质结构与性质
[物质结构与性质综合] 学法指导:《物质结构与性质》图片复习法 作者:吴乾环 来源:未知 日期:2020-03-05 12:42:30 点击:1369 所属专题:物质结构与性质
...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。一、电子的运动状态与电子的空间运动状态不同 电子的运动状态包括空间运动状态和自旋...
01.原子结构 02.核素原子一定含有质子和中子 【错误;反例如氕原子,只含有一个质子,...
注意:阴阳离子的配位数与化学式的关系 例如,CaF 2 晶胞中 晶体 类型(晶胞原型) 晶...
一、电子的运动状态与电子的空间运动状态不同 电子的运动状态包括 空间运动状态 和 自...
学习建议 高考中选修3的考试题型变化不大,常考“原子结构与元素的性质(基态微粒的电...
【问题1】为什么原子核外电子排布时,(n-1)d ns等出现能级交错现象? 【答】由于电...
1、高温陶瓷材料Si 3 N 4 晶体中键角N―Si―N > Si―N―Si(填“>”“<”“=”),原...
一、元素金属性、非金属性强弱的判断方法有哪些? 1.元素金属性强弱的判断方法 本质:...