
|
ѧϰСר�� |

|
ѧϰСר�� |
 [ע�������d] �ⶨԭ�����չ��ͷ������ʵ��ԭ����� ����:�°��� ��Դ:δ֪ ���ڣ�2016-03-11 21:54:00 �����771 ����ר�⣺����
[ע�������d] �ⶨԭ�����չ��ͷ������ʵ��ԭ����� ����:�°��� ��Դ:δ֪ ���ڣ�2016-03-11 21:54:00 �����771 ����ר�⣺����
�ڶ�ҳ...
 [ע�������d] ԭ�Ӻ�������Ų�������ƶ� ����:��� ��Դ:��ѧԭ�������IJ��� ���ڣ�2021-12-17 09:38:30 �����5847 ����ר�⣺��������Ų�����
[ע�������d] ԭ�Ӻ�������Ų�������ƶ� ����:��� ��Դ:��ѧԭ�������IJ��� ���ڣ�2021-12-17 09:38:30 �����5847 ����ר�⣺��������Ų�����
ԭ�Ӻ�����ӵ��Ų�������仯ѧ����������ء������˽�ԭ�Ӻ�������Ų����һֱ�Ǹ�����ѧ��ѧ�е�һ���ص㣬������ѧ����ͨ��ѧ��ѧ��Ҳ�����⡣ �Ա�һ�±Ƚ���Ӱ���һЩ����ѧ�̲ľͿ��Է��֣���˵���������ʱ�����Ƕ��õ�������ͼ��һ���DZ��ֵġ�ԭ�ӹ��...
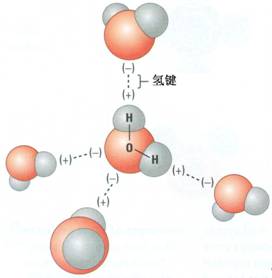 [ע�������d] ͨ���壺������ӵ��˶����Ų� ����:���� ��Դ:δ֪ ���ڣ�2021-12-17 09:20:20 �����2478 ����ר�⣺��������Ų�
[ע�������d] ͨ���壺������ӵ��˶����Ų� ����:���� ��Դ:δ֪ ���ڣ�2021-12-17 09:20:20 �����2478 ����ר�⣺��������Ų�
һ�����켣���롰���ᡱ ����������˶�״�������һ�ַ�ʽ�ǡ��켣��������2009��7��22�����Ϻ��۲���ȫʳ������8��23��24�������11��01��36�븴Բ���ⶼ�Ǹ���̫��������������˶��켣����Ԥ����(��ϧ�Ϻ����꣬û����)����ɫ���˶���˹̹����˹�쵼��ʵʩ��...
 [ע�������d] ��һ�����ܡ������ԡ���ԭ��֮��Ĺ�ϵ ����:³־�� ��Դ: ���ڣ�2015-05-26 18:34:59 �����13313 ����ר�⣺������ ������ ��ԭ��
[ע�������d] ��һ�����ܡ������ԡ���ԭ��֮��Ĺ�ϵ ����:³־�� ��Դ: ���ڣ�2015-05-26 18:34:59 �����13313 ����ר�⣺������ ������ ��ԭ��
һ�����壺 ��һ�����ܣ���̬�����Ի�̬ԭ��ʧȥһ������ת��Ϊ��̬��̬����������Ҫ������������һ������ �����ԣ�����ʾԪ�ص�ԭ��ʧȥ���ӵ�������Ȼ�ö���ܲ����ܡ� ��ԭ�ԣ���ָ����ʧ���ӵ�������һ��ͼ�̬�����ʾ��л�ԭ�ԡ� �����о����� ��һ�����ܣ�ijԪ��...
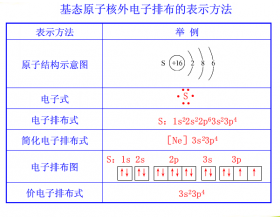 [ע�������d] ԭ�ӽṹ�ı�ʾ�����ܽ� ����:���� ��Դ:δ֪ ���ڣ�2021-03-08 09:18:46 �����2558 ����ר�⣺ԭ�ӽṹ03��ʾ����
[ע�������d] ԭ�ӽṹ�ı�ʾ�����ܽ� ����:���� ��Դ:δ֪ ���ڣ�2021-03-08 09:18:46 �����2558 ����ר�⣺ԭ�ӽṹ03��ʾ����
ע��Fe 2�� �ĺ�������Ų�ʽ�Ȳ���[Ar] 3d 4 4s 2 ��Ҳ����[AR] 3d 5 4s 1 ������[Ar] 3 d 6 ��1s 2 2s 2 2p 6 3s 2 3p 6 3d 6 Fe 3�� �ĺ�������Ų�ʽ��[Ar]3d 6 ��1s 2 2s 2 2p 6 3s 2 3p 6 3d 5 ��̬ͭ�ĺ�������Ų�ʽ��1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 1 һ��...
 [ע�������d] �縺�Խ�� ����:���� ��Դ:δ֪ ���ڣ�2015-02-02 22:56:38 �����2982 ����ר�⣺�縺��
[ע�������d] �縺�Խ�� ����:���� ��Դ:δ֪ ���ڣ�2015-02-02 22:56:38 �����2982 ����ר�⣺�縺��
���� �縺�ԣ�Electronegativity���ֳ�Ϊ��Ե縺�ԣ���Ƶ縺�ԡ��縺���ۺϿ����˵����ܺ͵������ܣ�����������˹��������������1932������縺�Եĸ��������ʾ������ͬԭ���γɻ�ѧ��ʱ�����������������ǿ������Ԫ�ص�ԭ���ڷ������������õ��ӵ�������ͨ����ϣ��...
 [ע�������d] �����ܽ�� ����:굱��� ��Դ:δ֪ ���ڣ�2015-02-01 17:09:34 �����7087 ����ר�⣺������
[ע�������d] �����ܽ�� ����:굱��� ��Դ:δ֪ ���ڣ�2015-02-01 17:09:34 �����7087 ����ר�⣺������
��1�����壺 ��̬ԭ�ӻ���̬����ʧȥһ����������Ҫ����С���� �� ��һ�����ܣ�I1) �����ڻ�̬����̬ԭ��ʧȥһ�����ӣ�����ʮ1 ����̬����������Ҫ�������� �ڶ������ܣ�I2) ���ɣ�1 ����̬��������ʧȥһ�������γ�ʮ2 ����̬����������Ҫ�������� ( 2 ��˵���� �� ������...
 [ע�������d] ����Ԫ�ص縺�Ե����� ����:��Сƽ ��Դ:δ֪ ���ڣ�2014-09-25 10:03:30 �����2042 ����ר�⣺�縺��
[ע�������d] ����Ԫ�ص縺�Ե����� ����:��Сƽ ��Դ:δ֪ ���ڣ�2014-09-25 10:03:30 �����2042 ����ר�⣺�縺��
���⣺�����ʽṹ�����ʡ�ģ��̲��ϵ�Ԫ�ص縺�Ժ�Щ���ݺ������ϲ鵽�IJ�ͬ��Ϊʲô�� ���ݵ縺�Ա�1.8�Ĵ��С���ж�Ԫ���ǽ������ǽ�����Sb��Bi��Pb�ǽ��������縺�Զ���1.9������1.8�� Si��Ti�縺�Զ���1.8��һ���ǽ�����һ���Ƿǽ�������ô���ͣ� P ��H �ĵ縺�Զ���1...
 [ע�������d] �縺��֪ʶ��Ӧ�� ����:����ƽ ��Դ:δ֪ ���ڣ�2014-09-14 21:12:17 �����4780 ����ר�⣺�縺��
[ע�������d] �縺��֪ʶ��Ӧ�� ����:����ƽ ��Դ:δ֪ ���ڣ�2014-09-14 21:12:17 �����4780 ����ר�⣺�縺��
1.�ж�Ԫ�ص����� һ������£��縺�Դ���1.8��Ϊ�ǽ���Ԫ�أ��縺��С��1.8��Ϊ����Ԫ�ء� 2.�жϻ�ѧ������ һ������£���Ԫ�ص縺�Բ�ֵ����1.7ʱ���γ����Ӽ�����Ԫ�ص縺�Բ�ֵС��1.7ʱ���γɹ��ۼ��� ���磺 Na�縺��0.9��Cl�縺��3.0������֮��IJ�ֵΪ2.1����1.7...
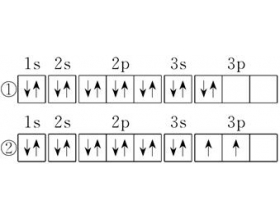 [ע�������d] ���ں��ع���Ľ���˵�� ����:��С�� ��Դ:δ֪ ���ڣ�2014-09-14 21:09:56 �����11816 ����ר�⣺���ع��� �ܼ�09 �����Ų�ʽ
[ע�������d] ���ں��ع���Ľ���˵�� ����:��С�� ��Դ:δ֪ ���ڣ�2014-09-14 21:09:56 �����11816 ����ר�⣺���ع��� �ܼ�09 �����Ų�ʽ
һ�����ع���Ķ��� �������Ų���ͬһ�ܼ��IJ�ͬ���ʱ����̬ԭ���еĵ����������ȵ���ռ��һ���������������״̬��ͬ�� ���ݺ��ع���Ķ��壬�ٲ����Ϻ��ع�����3P�ܼ����2������Ӧ�����ȵ���ռ��һ���������������״̬��ͬ���ڷ��Ϻ��ع���Ĺ涨�� �������ع����...
 ��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ�
��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ� ��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء�
��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء������ԭ���У��ڿ���ij������ʱ�������������Ӷ����ų����ÿ���������ԭ�Ӻ˶�����...
1.������ӹ��м����ܲ�? �ܲ���Ӳ�,������ԭ�Ӻ�Զ���IJ�ͬ,��������ɷ�Ϊ��һ����...
1��һ�����ӵ��˶�״̬Ҫ���ļ������������� ��Ӧ����������������ܲ�(���Ӳ�)�ǵ�...
...
��̬�ͼ���̬ ʲô�ǹ��ף� ���ף���ͬԪ�ص�ԭ�ӷ���ԾǨʱ�� ���� �� ��̬������̬ ...
���ֵ��ܼ�ͼֻ�Ǹ����Ƶ��ܼ�ͼ���ǰ�������������ӵ������̡� ������������...
��������Ų��Ƿdz�����˼�ġ��ڿ�ʼ��ʱ������ֵ���֮��֪��������ԭ��������...
�����Ʋ����ƣ��Ǹ��ʷֲ�ͼ �������ǵ�����ԭ�Ӻ���ռ���ֵĸ����ܶȷֲ�ͼ������...