
|
ѧϰСר�� |

|
ѧϰСר�� |
 [ע�������d] dz̸���������������ڸ��л�ѧ��Ӧ�� ����:����ƽ ��Դ:δ֪ ���ڣ�2020-10-26 16:33:07 �����1393 ����ר�⣺���������� �縺�� ������ �ǽ����� ������ ��ԭ��
[ע�������d] dz̸���������������ڸ��л�ѧ��Ӧ�� ����:����ƽ ��Դ:δ֪ ���ڣ�2020-10-26 16:33:07 �����1393 ����ר�⣺���������� �縺�� ������ �ǽ����� ������ ��ԭ��
�D���������� �л���ѧϰ������CH 2 =CH 2 ����ѡ�Լ��ϳ�CH 3 CH 2 CN���� ��ѧ�����������з���:CH 2 =CH 2 ��HCN��CH 3 CH 2 CN��HCN��һ �����Լ������ܺ�̼̼˫��������ӳɷ�Ӧ�����ַ����Ǵ���ġ����нΣ�ѧ��δ֪��Щ�����ʦ�ڽ�ѧ�����б������� ...
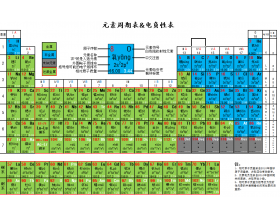 [ע�������d] Ԫ�����ڱ�������Ԫ��ע�����縺�����ݣ� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2021-12-29 14:10:28 �����7458 ����ר�⣺�縺�� Ԫ�ض���
[ע�������d] Ԫ�����ڱ�������Ԫ��ע�����縺�����ݣ� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2021-12-29 14:10:28 �����7458 ����ר�⣺�縺�� Ԫ�ض���
...
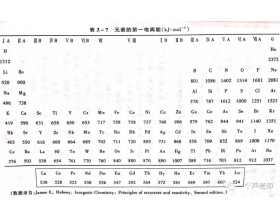 [ע�������d] �����ܡ��������ܺ͵縺�ԣ������������ʲô��ϵ�� ����:«�� ��Դ:δ֪ ���ڣ�2020-03-17 11:59:59 �����11451 ����ר�⣺������ �������� �縺��
[ע�������d] �����ܡ��������ܺ͵縺�ԣ������������ʲô��ϵ�� ����:«�� ��Դ:δ֪ ���ڣ�2020-03-17 11:59:59 �����11451 ����ר�⣺������ �������� �縺��
���������Ź��ںţ�һ��«��ʦ�����ߣ�«�� ������������������������ܵĸ��Ȼ���ٷ�������ѧ��ΪʲôҪ����縺�Եĸ�� 1�������� ʹԭ��ʧȥ���ӱ�������ӣ�Ҫ����һ���������Կ˷��˶Ե��ӵ�������ʹijԪ��1 mol ��̬��̬ԭ��ʧȥһ�������γ���һ�۵���̬��...
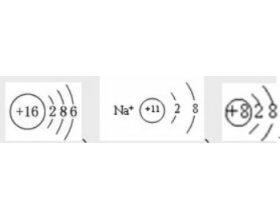 [ע�������d] ���������Ų��йظ������ ����:����ı ��Դ:δ֪ ���ڣ�2021-12-17 09:10:29 �����2337 ����ר�⣺��������Ų�
[ע�������d] ���������Ų��йظ������ ����:����ı ��Դ:δ֪ ���ڣ�2021-12-17 09:10:29 �����2337 ����ר�⣺��������Ų�
��ѧϰ�����ʽṹ�����ʡ�ѡ��ʱ��ѧ��δע�����ֱ�����������Ų����йظ���ͻᾭ������Ԫ���ƶ�ʧ��ѧ�������������ղ�ȷ������Ľ������⣬�������ŷ�����Ϊ�ˣ����������¸���������Թ������ 1�������ơ� ���ǵ�����ԭ�Ӻ��ⵥλ����ڳ���...
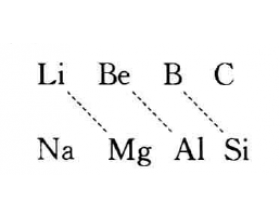 [̽������չa] ʲô�ǶԽ��߹���? ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2019-11-11 15:58:59 �����11707 ����ר�⣺�Խ��߹���
[̽������չa] ʲô�ǶԽ��߹���? ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2019-11-11 15:58:59 �����11707 ����ר�⣺�Խ��߹���
�����ڱ���ijһԪ�ص����ʺ������Ϸ������·�����һԪ�� ���ʵ������ԣ��ƶԽ��߹������������Խ����Եر�����Li�� Mg��Be��Al��B��Si����Ԫ��֮�䡣C��P��N��S��O��Cl û�����Եش������ֹ�ϵ�� (1) L i��Mg���ʵ������� ��Li��Mg�ڹ�����������ȼ�գ�ֻ���γ�������Li 2...
 [̽������չb] Ϊʲôԭ�Ӻ����������㲻����8��������㲻����18��? ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2021-12-17 09:36:05 �����11610 ����ר�⣺������ӷֲ��Ų� ����ԭ��
[̽������չb] Ϊʲôԭ�Ӻ����������㲻����8��������㲻����18��? ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2021-12-17 09:36:05 �����11610 ����ר�⣺������ӷֲ��Ų� ����ԭ��
ԭ�Ӻ���ĵ����Ų�������㲻����8��������㲻����18 �������ֹ��������ڵ����ܼ�������������ɵġ� �ɸ��Dz������ߵ�˳��1s, 2s2p, 3s3p, 4s3d4f��5s4d5p, 6s4f5d6p������֪����������ǵ��IJ㣬���ڵ����ܲ����֮ǰ����4s��4p����������ӣ����ҲֻΪ8����ͬ...
 [ע�������d] �õ����ܺ͵縺���жϽ����Ժͷǽ�����ǿ���������ݸ��ɿ�? ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2019-06-10 21:00:59 �����2091 ����ר�⣺������ �縺��
[ע�������d] �õ����ܺ͵縺���жϽ����Ժͷǽ�����ǿ���������ݸ��ɿ�? ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2019-06-10 21:00:59 �����2091 ����ר�⣺������ �縺��
�õ����ܺ͵縺���жϽ����Ժͷǽ�����ǿ���������ݸ��ɿ�? �𣺵縺��Ӧ�����жϽ����Ժͷǽ�����ǿ�����ɿ��� �ڶ�����.. Be�ĵ�һ������Ϊ899kJ��mol��B�ĵ�һ������Ϊ800kJ��mol��ԭ����Be��2s���ȫ����Bȴ��һ��p���ӣ����������p�����û�а�����N�ĵ�һ������Ϊ142...
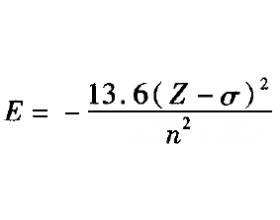 [ע�������d] ������ԭ��������ĵ����ڷ�Ӧ���Ƿ�����ʧȥ? ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2019-06-10 21:40:10 �����1396 ����ר�⣺����ԭ��
[ע�������d] ������ԭ��������ĵ����ڷ�Ӧ���Ƿ�����ʧȥ? ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2019-06-10 21:40:10 �����1396 ����ר�⣺����ԭ��
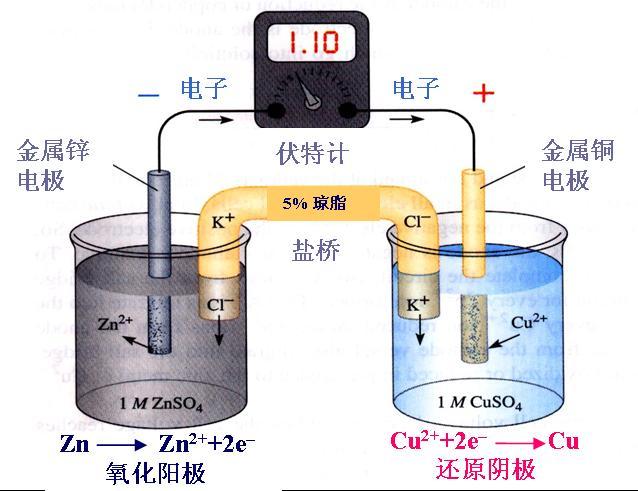
������ԭ��������ĵ����ڷ�Ӧ���Ƿ�����ʧȥ? �𣺲�һ��������ͭ�ĵ����Ų�ʽΪ1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 1 ��[ Ar]3d 10 4s 1 ������������4s��������3d����ʧȥ���ӳ�Ϊ����ʱȴ��ʧȥ4s���ӡ� ���Է��� ��ԭ����ʧȥ���ӳ�Ϊ���ӣ��˵���������������...
 [ע�������d] Fe�μӷ�Ӧʱ��Ϊʲô��ʧȥ�������ӣ�����������ߵĵ��ӣ� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2021-12-28 08:47:49 �����3964 ����ר�⣺����ʧ����
[ע�������d] Fe�μӷ�Ӧʱ��Ϊʲô��ʧȥ�������ӣ�����������ߵĵ��ӣ� ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2021-12-28 08:47:49 �����3964 ����ר�⣺����ʧ����
��̬ 26 Feԭ�ӵĺ�������Ų�ʽ��[Ar]3d 6 4s 2 ��Fe 2�� �ĺ�������Ų�ʽ�� [Ar]3d 6 ��ѧ�������ף�Feԭ�Ӳ��뷴Ӧʱ��Ϊʲô��ʧȥ 4s�ϵĵ��ӣ������Ǹ��ݡ�����Խ��Խ�ȶ���ԭ��ʧȥ������ߵ�3d�ϵĵ��ӣ� �����ԭ���У����Ӿ��е����� E �������������� n ...
 [ע�������d] Ϊʲô�ص��ܶȱ���С? ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2019-04-06 16:05:30 �����13684 ����ר�⣺������ ������ ���������ѻ�
[ע�������d] Ϊʲô�ص��ܶȱ���С? ����:��ѧ��ϰ�� ��Դ:δ֪ ���ڣ�2019-04-06 16:05:30 �����13684 ����ר�⣺������ ������ ���������ѻ�
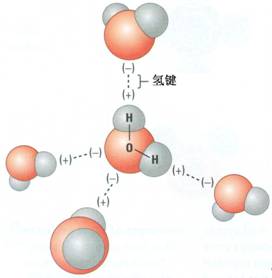
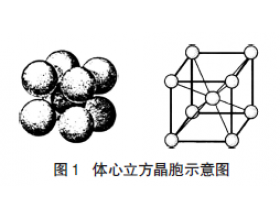
ͨ������£�ͬ����ĵ��ʵ��ܶ���������������������ڳ����£��Ƶ��ܶ�Ϊ 0.971g��cm-3����Ϊ 0.86g��cm-3��Ϊʲô�ص��ܶȷ�������С�� �ơ��صľ����������������ѻ�����ͼ 1����ÿ������������ 2 ��ԭ�ӡ� ���ݾ����ṹ�ɵó����ֽ��������ܶȵļ� �� ��ʽ�� M Ϊ...
 ��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ�
��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ� ��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء�
��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء������ԭ���У��ڿ���ij������ʱ�������������Ӷ����ų����ÿ���������ԭ�Ӻ˶�����...
1.������ӹ��м����ܲ�? �ܲ���Ӳ�,������ԭ�Ӻ�Զ���IJ�ͬ,��������ɷ�Ϊ��һ����...
1��һ�����ӵ��˶�״̬Ҫ���ļ������������� ��Ӧ����������������ܲ�(���Ӳ�)�ǵ�...
...
��̬�ͼ���̬ ʲô�ǹ��ף� ���ף���ͬԪ�ص�ԭ�ӷ���ԾǨʱ�� ���� �� ��̬������̬ ...
���ֵ��ܼ�ͼֻ�Ǹ����Ƶ��ܼ�ͼ���ǰ�������������ӵ������̡� ������������...
��������Ų��Ƿdz�����˼�ġ��ڿ�ʼ��ʱ������ֵ���֮��֪��������ԭ��������...
�����Ʋ����ƣ��Ǹ��ʷֲ�ͼ �������ǵ�����ԭ�Ӻ���ռ���ֵĸ����ܶȷֲ�ͼ������...